题目内容
【题目】(1)同分异构现象在有机化合物中是非常普遍的。下列各组化合物:
①CH3CH2CH2CH3和(CH3)2CHCH3; ②CH3CH2OH和CH3CH2CH2OH;
③CH3COOCH2CH3和CH3CH2CH2COOH; ④CH3CH=CHCH3和CH3CH2CH=CH2;
⑤![]() 和
和![]() 。其中互为同分异构体的是______________________(填序号)。
。其中互为同分异构体的是______________________(填序号)。
(2)下列5种有机化合物:乙酸乙酯(CH3COOCH2CH3)、苯酚(![]() )、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。
)、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH)。
①其中能与Na2CO3溶液反应产生气泡的是______________________。
②其中能与FeCl3溶液发生显色反应的是________________________。
③其中能发生银镜反应的是________________________。
④写出乙酸乙酯碱性条件水解反应的化学方程式____________________________。
(3)①蛋白质是维持生命的重要物质,它是由_____________________通过缩聚反应生成的一类高分子化合物;氨基酸因分子中含有的官能团是____________________和____________________,而具有__________________性。
②2008年,三鹿婴幼儿奶粉由于人为添加三聚氰胺,导致长期食用该奶粉的部分婴幼儿出现肾结石病。三聚氰胺的结构简式如下图所示。
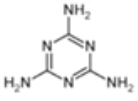
请你预测三聚氰胺在核磁共振氢谱图(1H核磁共振谱图)中会出现____________________个峰;三聚氰 胺中氮元素的质量分数为______________________(结果用百分数表示,并保留一位小数),添加三聚氰胺会使食品中蛋白质的含量虚高。
【答案】 ①③④ CH3COOH 苯酚 CH3CHO CH3COOCH2CH3 + NaOH![]() CH3COONa + CH3CH2OH 氨基酸 羧基 氨基 两 1 66.7%
CH3COONa + CH3CH2OH 氨基酸 羧基 氨基 两 1 66.7%
【解析】(1)①属于碳链异构,②是同系物,③是官能团异构,④是位置异构,⑤的分子式不同,故属于同分异构体的是①③④。
(2)①能与Na2CO3溶液反应产生气泡的是CH3COOH;②能与FeCl3溶液发生显色反应的是苯酚;③醛基可以发生银镜反应,故可以发生银镜反应的是CH3CHO;④乙酸乙酯碱性条件水解反应的化学方程式为:CH3COOCH2CH3 + NaOH![]() CH3COONa + CH3CH2OH。
CH3COONa + CH3CH2OH。
(3)①蛋白质是由氨基酸通过缩聚反应生成的,氨基酸含有的官能团是氨基和羧基,羧基显酸性,氨基显碱性,因而氨基酸具有两性。②由三聚氰胺的结构式可知,只有一种氢原子,故在核磁共振氢谱上只出现一种峰;三聚氰胺的分子式为C3N6H6,N元素的质量分数为14×6÷126×100%=66.7%。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
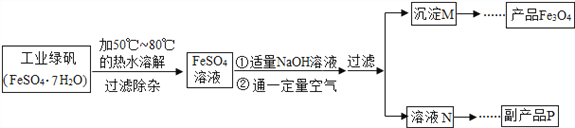
口算与应用题卡系列答案【题目】某化学兴趣小组对Fe3O4产生了兴趣,从参考资料中找到了氧化沉淀法生产复印用高档Fe3O4粉的工艺流程简图:
 【查阅资料】
【查阅资料】
资料一:硫酸亚铁在不同温度下的溶解度如表所示:
温度/℃ | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
资料二:Fe(OH)2受氧气氧化反应原理为:4Fe(OH)2 +2H2O+O2=4Fe(OH)3
资料三:获得Fe3O4的反应原理为:Fe(OH)2 + 2Fe(OH)3 ![]() Fe3O4+4H2O
Fe3O4+4H2O
Ⅰ【问题讨论】
(1)溶解时,用50℃至80℃的热水目的是__________________________________________。
(2)副产品P是___________________________。
(3)为了得到纯净的产品,过滤、洗涤后进行的具体操作过程为______________________________、干燥
Ⅱ【组成确定】
资料显示:①铁的氢氧化物在受热时分解生成铁的氧化物(化合物不变);
②Fe2O3和CO反应是随温度升高而逐步进行的,先生成Fe3O4,再生成FeO(黑色),最后生成Fe。
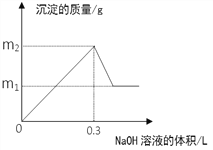
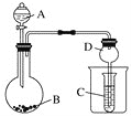
为确定用以上方法制得的四氧化三铁的纯度,同学们称取了23.28g该Fe3O4样品设计下列实验进行探究。
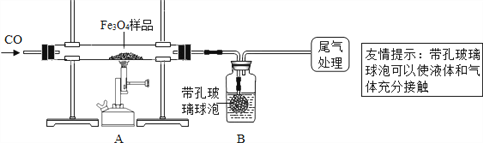
(1)该组同学欲通过称量B装置反应前后的质量变化来计算确认该Fe3O4样品中的杂质。B中的最佳试剂是_______________________(填序号)。
A.澄清石灰水 B.氢氧化钠浓溶液 C.稀盐酸 D.水
(2)上述实验过程中,CO气体除作为反应物外,能起到的作用还有:
①实验开始时,排尽装置中的空气,防止加热时发生爆炸;
②停止加热后,继续通CO气体,防止生成物被氧化,以及B中的溶液倒吸入A中;且可以_____________________________,以提高实验的精确度。
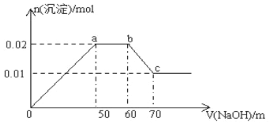
(3)利用仪器测定并绘制出反应过程中
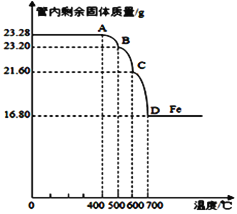
①该Fe3O4样品中含有的杂质成分______________________(填化学式)
②计算样品中Fe3O4的质量分数(写出必要的计算过程)。 _____________