题目内容
16.在8NH3+3Cl2→6NH4Cl+N2反应中,若有10.2gNH3被氧化,则反应用去的氯气在标准状况下体积为( )| A. | 5.04L | B. | 6.72L | C. | 20.16L | D. | 40.32L |
分析 被氧化的氨气生成N2,根据原子守恒计算氮气的物质的量,再根据方程式计算氯气的物质的量,进而计算参加反应氯气的体积.
解答 解:10.2g氨气的物质的量=$\frac{10.2g}{17g/mol}$=0.6mol,氨气被氧化生成氮气,根据N原子守恒可知生成氮气的物质的量=$\frac{0.6mol}{2}$=0.3mol,由方程式8NH3+3Cl2═6NH4Cl+N2可知参加反应氯气为0.3mol×3=0.9mol,故参加反应氯气的体积=0.9mol×22.4L/mol=20.16L,
故选C.
点评 本题考查化学方程式的有关计算、氧化还原反应有关计算,难度不大,利用电子转移守恒计算氯气的物质的量更简单.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
5.下列各组物质间的反应与反应类型不相符的是( )
| A. | 乙烯与溴水(加成反应) | B. | 苯与液溴(取代反应) | ||
| C. | 乙醇与乙酸的酯化反应(取代反应) | D. | 乙醇与氧气(取代反应) |
4.根据A-J在周期表中的位置,用元素符号或化学式回答下列问题:
(1)J的原子结构示意图为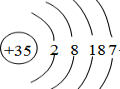 .
.
(2)表中元素,化学性质最不活泼的是Ne,只有负价而无正价的是F,氧化性最强的单质是F2,还原性最强的单质是Na.
(3)最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是HClO4,呈两性的是Al(OH)3.
(4)A分别与D、E、F形成的化合物中,最稳定的是NH3.
(5)在C、D、G、H中,原子半径最大的是Al.
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H | ||||
| 4 | J |
 .
.(2)表中元素,化学性质最不活泼的是Ne,只有负价而无正价的是F,氧化性最强的单质是F2,还原性最强的单质是Na.
(3)最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是HClO4,呈两性的是Al(OH)3.
(4)A分别与D、E、F形成的化合物中,最稳定的是NH3.
(5)在C、D、G、H中,原子半径最大的是Al.
1.化学与社会、生活密切相关,下列有关说法不正确的是( )
| A. | 利用清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 食品添加剂种类很多,其中的一种为苯甲酸钠,它是苯的一种同系物所对应的钠盐 | |
| C. | 某些蔬菜和水果在人体代谢后,生成碱性物质,所以称为碱性食物 | |
| D. | 抗酸药的种类很多,如碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝、氢氧化镁等 |
8.现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p5;②1s22s22p63s23p3;③1s22s22p33s23p4;④1s22s22p5.则下列有关比较中正确的是( )
| A. | 第一电离能:④>①>②>③ | B. | 原子半径:①>③>②>④ | ||
| C. | 电负性:④>③>②>① | D. | 最高正化合价:④=①>③>② |
5.下列电子式正确的是( )
| A. | H2O2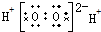 | B. | HClO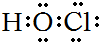 | C. | MgCl2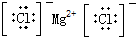 | D. | CCl4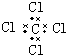 |