题目内容
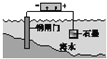
【题目】已知反应2NO2N2O4(g) H<0。将一定量的NO2充入注射器中并密封,改变活塞位置的过程中,气体透光率随时间的变化如图所示(气体颜色越深,透光率越小)。下列说法不正确的是
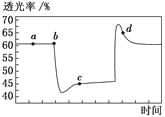
A.b 点的操作是压缩注射器
B.c 点与a点相比,c(NO2)增大、c(N2O4)减小
C.d 点:υ(正)<υ(逆)
D.若在c点将温度降低,其透光率将增大
【答案】B
【解析】
温度不变时,压缩体积,压强增大,虽然平衡正向移动,但是NO2和N2O4的浓度均增大,颜色变深,透光率降低,因此b点为压缩体积的点,同理透光率突然增大,是拉伸,扩大了体积。
A.b点开始透光率陡然下降,压缩体积,NO2浓度增大,导致透光率降低,A正确;
B.图中c点为压缩体积后的再次建立过程平衡,由于压缩体积,因此NO2和N2O4的浓度均增大,因此c(NO2)比a点大,c(N2O4)也同样应比原来的大,B不正确;
C.d点透光率正在减小,c(NO2)增大,平衡逆向移动,则v(正)<v(逆),C正确;
D.该反应为放热反应,降低温度,平衡正向移动,c(NO2)降低,则透光率将增大,D正确;
故选B。

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案【题目】现有 A、B、C、D、E、F 六种短周期主族元素,其相关性质信息如下:
元素 | 相关信息 |
A | 地壳中含量最多的金属元素 |
B | 原子核外电子数和周期序数相等 |
C | 最外层电子数是次外层电子数的 3 倍 |
D | 最高正价与最低负价代数和为 4,常温下单质为固体 |
E | 在短周期元素中,原子半径最大 |
F | M 层比L 层少 1 个电子 |
请根据上述信息,完成下列问题:
(1)请给出元素 D 在元素周期表中的位置:________。
(2)请将 A、D、E、F 四种元素的简单离子按照离子半径由大到小排序(用离子符号表示):__________。
(3)请给出化合物 BFC 的电子式:______。
(4)用电子式表示 E 与 F 形成化合物 EF 的过程:______。
(5)请将 A、D、F 三种元素的最高价氧化物对应的水化物按照酸性由强到弱排序(用化学式表示):__________。
(6)元素 A 的单质常用于野外焊接钢轨,请写出该反应的化学方程式:________。
(7)单质 A 能溶于 E 的最高价氧化物对应水化物的水溶液,请给出该反应的离子方程式:_____________。