题目内容
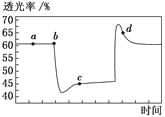
【题目】已知:2CrO42-+2H+Cr2O72-+H2O。25℃时,调节初始浓度为1.0molL-1的Na2CrO4溶液的pH,测定平衡时溶液中c(Cr2O72-)和c(H+),获得如图所示的曲线。下列说法不正确的是( )

A.平衡时,pH越小,c(Cr2O72-)越大
B.A点CrO42-的平衡转化率为50%
C.A点CrO42-转化为Cr2O72-反应的平衡常数K=1014
D.平衡时,若溶液中c(Cr2O72-)=c(CrO42-),则c(H+)>2.0×10-7molL-1
【答案】D
【解析】
A、由图可知氢离子浓度越大,![]() 越大,所以pH越小,
越大,所以pH越小,![]() 越大,选项A正确;
越大,选项A正确;
B、由图可知A点时![]() 的平衡浓度为
的平衡浓度为![]() ,所以转化的
,所以转化的![]() 的浓度为:
的浓度为:![]() ,则A点
,则A点![]() 的平衡转化率为
的平衡转化率为![]() ,选项B正确;
,选项B正确;
C、![]() 的平衡常数为:
的平衡常数为: ,选项C正确;
,选项C正确;
D、平衡时,若溶液中![]() ,而
,而![]() ,所以
,所以![]() ,而图中
,而图中![]() 时,对应氢离子的浓度为
时,对应氢离子的浓度为![]() ,则溶液中
,则溶液中![]() ,则
,则![]() ,选项D错误。
,选项D错误。
答案选D。

【题目】用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,
实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
1 | 25.00 | 24.41 |
2 | 25.00 | 24.39 |
3 | 25.00 | 24.60 |
回答下列问题:
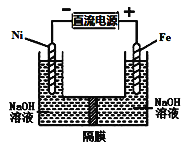
(1)如图中甲为___________滴定管,乙为_________ 滴定管(填“酸式”或“碱式 ”)
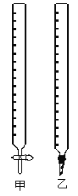
(2)实验中,需要润洗的仪器是:________________________
(3)取待测液NaOH溶液25.00ml 于锥形瓶中,使用酚酞做指示剂。滴定终点的判断依据是________________________________________
(4)若滴定前,滴定管尖端有气泡,滴定后气泡消失,将使所测结果____________(填“偏高”“偏低”“不变”,下同);若读酸式滴定管读数时,滴定前仰视读数,滴定后正确读数,则所测结果___________。
(5) 未知浓度的NaOH溶液的物质的量浓度为_____________mol/l。