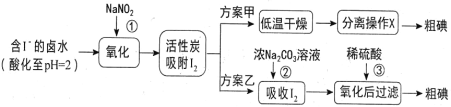
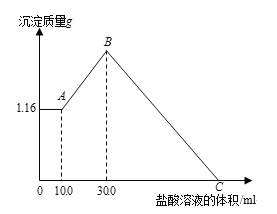
题目内容
【题目】某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
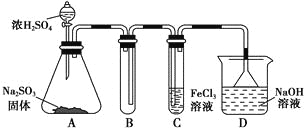
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在________中,再加水稀释,这样操作的目的是________,操作中不需要的仪器有________(填入正确选项前的字母)。
a.药匙 b.烧杯 c.石棉网 d.玻璃棒 e.坩埚
(2)通入足量SO2时,C中观察到的现象为______________________________。
(3)根据以上现象,该小组同学认为SO2与FeCl3溶液发生了氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:___________________________;
②请设计实验方案检验有Fe2+生成:__________________________________;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法________(填“合理”或“不合理”),理由是_______________________________________________________________。
(4)D装置中倒置漏斗的作用是______________________________________。
(5)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有________(填入正确选项前的字母)。
a.浓H2SO4b.酸性KMnO4溶液
c.碘水 d.NaCl溶液
【答案】浓盐酸 抑制氯化铁水解 ce 溶液由棕黄色变为浅绿色 2Fe3++SO2+2H2O=SO42-+4H++2Fe2+ 取C中反应后的溶液,向其中滴入KSCN溶液,不变红,再加入新制的氯水(或H2O2溶液等),溶液变红 不合理 硝酸可以将溶解的SO2氧化为H2SO4,干扰实验 使气体充分吸收,防止溶液倒吸 bc
【解析】
(1)氯化铁在水溶液中易发生水解,因此配制氯化铁溶液时,一般先把氯化铁晶体溶于浓盐酸中,再加水稀释,以抑制其水解。配制溶液在烧杯中进行,不需要石棉网和坩埚;
(2)SO2与FeCl3溶液发生氧化还原反应,Fe3+被还原为Fe2+,溶液由棕黄色变为浅绿色;
(3)①SO2与FeCl3溶液反应生成硫酸和FeCl2,离子方程式为2Fe3++SO2+2H2O=SO42-+4H++2Fe2+;
②检验Fe2+时要排除Fe3+的干扰,即先加KSCN溶液,在确认溶液中不存在Fe3+的情况下,加入氯水等氧化剂,若有Fe2+,则溶液变红;
③向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,该沉淀可能是硝酸将溶解的SO2氧化为H2SO4,从而生成白色沉淀,所以不合理;
(4)倒置的漏斗与水有较大的接触面积,可使气体充分吸收并防止溶液倒吸;
(5)验证SO2具有还原性,要求用具有氧化性的试剂,能与SO2发生氧化还原反应且有明显现象,答案为bc。

 阅读快车系列答案
阅读快车系列答案【题目】空气中的硫酸盐会加剧雾霾的形成,我国科学家用下列实验研究其成因:反应室底部盛有不同吸收液。将SO2和NO2按一定比例混合,以N2或空气为载气通入反应室,相同时间后,检测吸收液中SO42-的含量数据如下表所示,下列说法正确的是
反应室 | 载气 | 吸收液 | SO42-含量 | 数据分析 |
① | N2 | 蒸馏水 | a | b |
② | 3%氨水 | b | ||
③ | 空气 | 蒸馏水 | c | |
④ | 3%氨水 | d |
A.实验表明:酸性环境下,更有利于硫酸盐的形成
B.本研究表明:硫酸盐的形成主要与N2有关
C.反应室①中可能发生反应:SO2+2NO2+2H2O=H2SO4+2HNO2
D.燃煤产生的气体盲目排放会引起酸雨但不会加剧雾霾形成