��Ŀ����
����Ŀ��Ϊ��̽����ѧ��Ӧ���ʺͻ�ѧ��Ӧ�ȵ��й����⣬ij�о�С�����������ʵ�飺
��� | ��Ӧ�¶ȣ��� | C(H2O2)/mol-L | V(H2O2)/mL | M(MnO2)/g | t/min |
1 | 20 | 2 | 10 | 0 | t1 |
2 | 20 | 2 | 10 | 0.1 | t2 |
3 | 20 | 4 | 10 | 0.1 | t3 |
4 | 40 | 2 | 10 | 0.1 | t4 |
(1)���ʵ��2��ʵ��3��Ŀ�����о�_______�Ի�ѧ��Ӧ���ʵ�Ӱ�졣
(2)Ϊ�о��¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬���Խ�ʵ��_____��ʵ��____���Աȣ�����ţ���
(3)��ʵ��1��ʵ��2���Աȣ�t1____t2���>������<����=������
II.��KI��FeCl3��ӦΪ��(2Fe3++2I-![]() 2Fe2++I2)���ʵ�飬̽���˷�Ӧ����һ�����ȡ���ѡ�Լ�����0.1mol��L-1KI��Һ ��0.1mol��L-1 FeCl3��Һ��0.1mol��L-1 FeCl2��Һ ��0.1mol��L-1 HCl��Һ��0.1mol��L-1 FeSCN��Һ�� CCl4
2Fe2++I2)���ʵ�飬̽���˷�Ӧ����һ�����ȡ���ѡ�Լ�����0.1mol��L-1KI��Һ ��0.1mol��L-1 FeCl3��Һ��0.1mol��L-1 FeCl2��Һ ��0.1mol��L-1 HCl��Һ��0.1mol��L-1 FeSCN��Һ�� CCl4
ʵ�鲽�裺
��1��ȡ5mL0.1mol��L-1KI��Һ,�ٵμӼ���0.1mol��L-1 FeCl3��Һ
��2����ַ�Ӧ����Һ�ֳ����ݣ�
��3��ȡ����һ�ݣ����Լ��ޣ���CCl4������ɫ��˵����Ӧ���ɵ⣻
��4����ȡһ�ݣ����Լ�_______������ţ�������___________��˵���˷�Ӧ����һ�����ȡ�
���𰸡� H2O2��Ũ�� 2 4 �� �� ��Һ����Ѫ��ɫ
��������I����ʵ����Ҫ���鷴Ӧ�¶ȡ���Ӧ���Ũ�ȡ������������Ի�ѧ��Ӧ���ʵ�Ӱ�죬�ڽ��жԱ�ʵ��ʱ��Ϊ�˾��пɱ���ֻ�ܸı�һ��������������������ͬ�������Ƚϲ������塣
��1��ʵ��2��ʵ��3��Ӧ�¶ȡ���������������ͬ����Ӧ��H2O2��Ũ�Ȳ�ͬ���ʱ����������Ŀ�����о�H2O2��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�졣
��2��Ҫ�о��¶ȶԷ�Ӧ���ʵ�Ӱ�죬���뱣�ִ�������������Ӧ���Ũ����ͬ����ʹ�¶Ȳ�ͬ����ѡ�� (3)�� (4)���Ա����顣
��3��ʵ��1��ʵ��2���¶ȡ���Ӧ���ũ�Ⱦ���ͬ��ʵ��1��������ʵ��2��ʹ���������������������Լӿ췴Ӧ���ʣ���ʵ��2�����ʽϿ죬ʱ��̣�t1��t2��
II��ʵ��IIͨ�����鷴Ӧ��ϵ�з�Ӧ����������Ƿ�ͬʱ������̽���÷�Ӧ�Ƿ�Ϊ���淴Ӧ���Ӷ�̽���˷�Ӧ����һ��������
ȡ����һ�ݷ�Ӧ�����Һ�����Լ�CCl4����CCl4������ɫ��˵����Ӧ���ɵ⣬���Ǽ���������Ĵ�������ȡһ����Һ������KSCN��Һ����Һ��Ѫ��ɫ��֤��������Fe��SCN��3��Ҳ��֤���˷�Ӧ��ϵ������Fe3+�Ĵ��ڣ�Ҳ����˵��Ӧ�з�Ӧ��δ��ȫ��Ӧ�������������֤���˸÷�ӦΪ���淴Ӧ������Ӧ����һ�����ȡ�

 ͬ��������ϰϵ�д�
ͬ��������ϰϵ�д� �ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�
�ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�����Ŀ���о��������������Դ������������������Ҫ�����塣��ش��������⣺
��1����2 L�ܱ������ڣ� 800 ��ʱ��Ӧ2NO(g)��O2(g) ![]() 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
����ͼ��ʾA�㴦v��___(�>������<����������ͬ)v����A�㴦v��___B�㴦v����
����ͼ��ʾ�����ߣ����б�ʾNO2�ı仯��������________����a��b��c��d����ĸ������O2��ʾ2 s�ڸ÷�Ӧ������v��________��
��2����֪��ѧ��ӦN2��3H2![]() 2NH3�������仯��ͼ��ʾ��
2NH3�������仯��ͼ��ʾ��
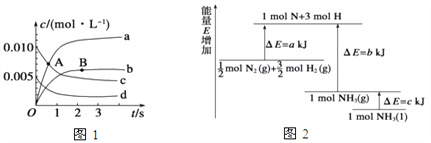
��1 mol N��3 mol H����1 mol NH3(g)��______�����Ĺ���(����ա����ͷš�)����![]() mol N2(g)��
mol N2(g)��![]() mol H2(g)����1 mol NH3(g)����________(����ա����ͷš�)_______kJ�������ú���ĸa��b��c�Ĺ�ϵʽ�����
mol H2(g)����1 mol NH3(g)����________(����ա����ͷš�)_______kJ�������ú���ĸa��b��c�Ĺ�ϵʽ�����
����Ŀ���Ӻ������̽���۱�������Ҫ�Ļ�ѧѧ����������FeCl3��ҺΪʵ���о�����̽�������������֮��ĸ��Ӷ����ԡ�ʵ�����£�
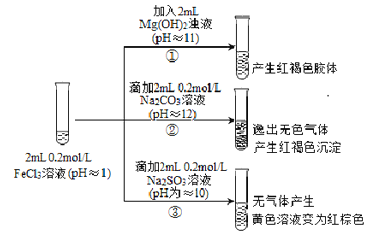
��1�����з�Ӧ�����ӷ���ʽ��_________________��
��2�������ݳ�����ɫ������_______________��
��3�����ڢ��е�ʵ������ͬѧ�������²⣬��������ʵ�飺
��ȡ���еĺ���ɫ��Һ�������������������ữ��BaCl2��Һ��������ɫ������ �ó����ۣ�FeCl3��Na2SO3������������ԭ��Ӧ�����ӷ���ʽ��______________��
������Ϊ��ʵ�鲻�Ͻ���������Ʋ�����ʵ�飬֤ʵ�˼Ľ�������ȷ�ġ���ʵ�鷽����ȡ����������Һ��������__________���ӵļ��顣
��4��������ʵ���������ͬѧ�Ƕ�pH��8��1mol/LNaF��Һ��FeCl3��Һ���ʱ����������˺��沢����ʵ�飺
ʵ����������� | ����2mL0.2mol/L FeCl3��Һ�е���2mL1mol/LNaF��Һ����Һ����ɫ |
����2mL0.2mol/L FeCl3��Һ�е���2mL����ˮ����Һ��ɫ��dz |
�ݵ�ʵ��Ŀ����___________��
��Ϊ̽��������Һ����ɫ��ԭ��������ʵ�飺
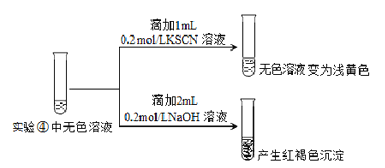
������ʾ��FeF3��ҺΪ��ɫ��
��ƽ���ƶ�ԭ�����ͺ��ɫ����������ԭ��_______________��
��5������ʵ�飬FeCl3��Һ���������֮��ķ�Ӧ�Ķ�������_____________________�йء�



