题目内容
【题目】在如图中表示的是有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物。(反应条件图中已省略)。
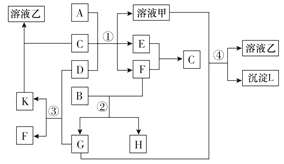
(1)A、C代表的物质分别为______、______(填化学式);
(2)反应①中的C、D均过量,该反应的化学方程式是 _____________;
(3)反应②中,若B与F物质的量之比为4:3,G、H物质的量之比为______;
(4)反应④的离子方程式为______________。
【答案】Al H2O 2H2O+2Na2O2=4NaOH+O2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 1:1 CO2+2OH-=CO32-+H2O 、2AlO2-+CO2+3H2O=2Al(OH)3↓+ CO32-
【解析】
题干信息:A为常见的金属单质,B为非金属单质(一般是黑色粉末)推断为C (碳)单质,C是常见的无色无味液体可以推断C为H2O,D是淡黄色的固体化合物判断为Na2O2,E、F为O2和H2,二者反应生成水,A是常见金属,与另一种固体在水中反应生成O2和H2,则该金属A为Al单质;固体D为Na2O2,能与水和CO2反应,则G为CO2;说明K为Na2CO3,F为O2,则E为H2;题给信息黑色单质B(C单质)与F(O2)反应得到G(CO2);C和O2反应可生成CO2和CO,则H为CO;A、C、D反应产生E、F、溶液甲,由于A是Al,C是H2O,D是Na2O2,E为H2,F是O2,甲是NaAlO2;G是CO2,其与过氧化钠反应生成碳酸钠和氧气,碳酸钠溶于水中得到的溶液乙为碳酸钠溶液。溶液甲为NaOH和NaAlO2的混合液,将CO2通入甲溶液,反应产生Al(OH)3沉淀和Na2CO3溶液,则沉淀L是Al(OH)3,结合物质的性质解答该题。
根据上述分析可知:A是Al,B是C,C是H2O,D是Na2O2,E是H2,F是O2,G是CO2,H是CO,K是Na2CO3,甲是NaAlO2,乙是NaHCO3,L是Al(OH)3。
(1)依据推断可知,A是Al,C是H2O;
(2)反应①中的C、D均过量,生成的氢氧化钠溶液能和A完全反应,该反应的化学方程式是:2Na2O2+2H2O=4NaOH+O2↑、2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(3) B是C,F是O2,若二者按物质的量之比为4:3发生反应,根据反应前后各种元素的原子个数相等,可得反应的方程式为:4C+3O2![]() 2CO+2CO2,则反应产生的CO2、CO的物质的量的比n(CO2):n(CO)=2:2=1:1;
2CO+2CO2,则反应产生的CO2、CO的物质的量的比n(CO2):n(CO)=2:2=1:1;
(4)反应④是向氢氧化钠和偏铝酸钠混合溶液中通入二氧化碳,发生反应生成氢氧化铝沉淀和碳酸钠,反应④的离子方程式为CO2+2OH-=CO32-+H2O 、2AlO2-+CO2+3H2O=2Al(OH)3↓+ CO32-。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某实验小组用100mL0.50mol/LNaOH溶液与60mL0.50mol/L硫酸进行中和热的测定。装置如图所示,回答下列问题:
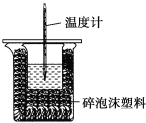
(1)若实验共需要400mLNaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体____g。
(2)图中装置缺少的仪器是____。
(3)硫酸稍过量的原因是____。
(4)请填写下表中的平均温度差:
实验 次数 | 起始温度T1/℃ | 终止温度 T2/℃ | 平均温度差 (T2-T1)/℃ | ||
HCl | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ____ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
(5)近似认为0.50 mol/L NaOH溶液与0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容为c=4.18J/(g℃)则上述实验中和热ΔH=___(取小数点后一位)
(6)上述实验结果与57.3kJ/mol有偏差产生偏差的原因可能是____
A.量取NaOH溶液时仰视读数
B.为了使反应充分,可以向酸中分次加入碱
C.实验装置保温隔热效果差
D.用铜丝代替玻璃棒搅拌