题目内容
7.有一种绿色粉末状的纯净物M,在加热条件下分解,生成三种物质A、B、C.①无色气体A通过炽热的焦炭后转化为气体D;
②黑色粉末B在加热条件下与D反应,生成红色固体E,同时放出无色气体A;
③A与石灰沙浆中的F反应,能够生成白色坚固的固体G.
试回答:
(1)写出绿色粉末M的化学式Cu2(OH)2CO3.
(2)写出上面反应①、②、③的化学方程式:
①CO2+C$\frac{\underline{\;高温\;}}{\;}$ 2CO;
②CuO+CO $\frac{\underline{\;高温\;}}{\;}$Cu+CO2;
③CO2+Ca(OH)2=CaCO3↓+H2O.
分析 根据常见的黑色粉末有:氧化铜、碳、二氧化锰等,红色物质有氧化铁、铜、红磷等,使石灰水变浑浊的气体是二氧化碳,黑色粉末混合物加热会生成红色的物质和二氧化碳,所以红色物质是铜,黑色物质是碳和氧化铜,无色气体A通过炽热的焦炭后转化为气体D,则A应为CO2,D为CO,黑色粉末B在加热条件下与D反应,生成红色固体E,同时放出无色气体A,该反应为氧化铜与一氧化碳的反应,所以B为CuO,E为Cu,A与石灰沙浆中的F反应,能够生成白色坚固的固体G,则F为Ca(OH)2,G为CaCO3,根据元素守恒,可知M中有铜元素,M分解生成氧化铜和二氧化碳,根据绿色粉末状的这一特征,可推出M为Cu2(OH)2CO3,据此答题.
解答 解:根据常见的黑色粉末有:氧化铜、碳、二氧化锰等,红色物质有氧化铁、铜、红磷等,使石灰水变浑浊的气体是二氧化碳,黑色粉末混合物加热会生成红色的物质和二氧化碳,所以红色物质是铜,黑色物质是碳和氧化铜,无色气体A通过炽热的焦炭后转化为气体D,则A应为CO2,D为CO,黑色粉末B在加热条件下与D反应,生成红色固体E,同时放出无色气体A,该反应为氧化铜与一氧化碳的反应,所以B为CuO,E为Cu,A与石灰沙浆中的F反应,能够生成白色坚固的固体G,则F为Ca(OH)2,G为CaCO3,根据元素守恒,可知M中有铜元素,M分解生成氧化铜和二氧化碳,根据绿色粉末状的这一特征,可推出M为Cu2(OH)2CO3,
(1)由上面的分析可知,M为Cu2(OH)2CO3,故答案为:Cu2(OH)2CO3;
(2)①二氧化碳和碳反应生成一氧化碳,反应的化学方程式为:CO2+C$\frac{\underline{\;高温\;}}{\;}$ 2CO;
②氧化铜和一氧化碳反应生成铜和二氧化碳,反应的化学方程式为:CuO+CO $\frac{\underline{\;高温\;}}{\;}$Cu+CO2;
③二氧化碳和氢氧化钙反应生成碳酸钙和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O,
故答案为:CO2+C$\frac{\underline{\;高温\;}}{\;}$ 2CO;CuO+CO $\frac{\underline{\;高温\;}}{\;}$Cu+CO2;CO2+Ca(OH)2=CaCO3↓+H2O.
点评 在解此类方程式的书写题时,首先确定反应原理,然后再依据原理找出反应物、生成物和反应条件,根据方程式的书写规则书写方程式.

| A. | 镁条作负极,电极反应:Mg-2e-=Mg2+ | |
| B. | 铝片作负极,电极反应:Al+4OH--3e--=[Al(OH)4]- | |
| C. | 电流从Al电极沿导线流向Mg电极 | |
| D. | 铝片上有气泡产生 |
| A. | O<S<Se<Te | B. | C<N<O<F | C. | P<S<O<F | D. | K<Na<Mg<Al |
| A. | 氮气的电子式  | |
| B. | Mg2+的结构示意图 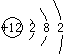 | |
| C. | NH3的结构式 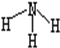 | |
| D. | 用电子式表示溴化氢的形成过程为: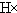 + +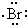 → →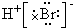 |
(1)已知:①H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H1═-285.8KJ•mol-1
②CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H1═-725.5KJ•mol-1
则CO2(g)+3H2(g)═CH2OH(l)+H2O(l)的反应热△H═-131.9KJ/mol;.
(2)某研究小组用CO合成甲醇:CO(g)+2H2(g)═CH3OH(l)△H<0,将三组混合气体分别通入到三个2L恒容密闭容器中进行反应,得到如下三组实验数据:
| 实验组 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | 达到平衡所需的时间/min | ||||
| CO | H2 | CH3OH | CO | H2 | CH3OH | |||
| 1 | 650℃ | 2.0 | 6.0 | 0 | 1.0 | 5 | ||
| 2 | 900℃ | 2.0 | 6.0 | 0 | 1.2 | 2 | ||
| 3 | 650℃ | 1.0 | 4.0 | 2.0 | a | b | c | t |
(3)已知CO的转化率(a)与温度(T)、压强(p)的关系如右图所示:
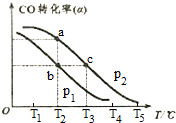
①p1<p2(填“<”、“>”或“═”),先升高温度,后增大压强,能否实现b点到c点的转化?能(填“能”或“不能”),原因是先升高温度,后增大压强,一氧化碳转化率先减小后增大,可以到达C点一氧化碳转化率不变.
②a、c两点的反应速率为v1<v2(填“<”、“>”或“═”)
③在不改变反应物用量的情况下,为提高CO的转化率可采取的措施是:增大氢气浓度,增大压强、降低温度(答出三条措施)
 肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.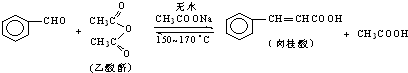
药品物理常数
| 苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
| 溶解度(25℃,g/100g水) | 0.3 | 遇热水水解 | 0.04 | 互溶 |
| 沸点(℃) | 179.6 | 138.6 | 300 | 118 |
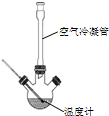
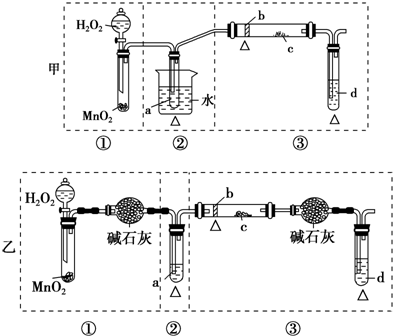
合成:反应装置如图所示.向三颈烧瓶中先后加入研细的无水醋酸钠、苯甲醛和乙酸酐,振荡使之混合均匀. 在150~170℃加热1小时,保持微沸状态.
(1)空气冷凝管的作用是使反应物冷凝回流.
(2)该装置的加热方法是空气浴(或油浴).加热回流要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是乙酸酐蒸出,反应物减少,平衡左移.
(3)不能用醋酸钠晶体(CH3COONa•3H2O)的原因是乙酸酐遇热水水解.
粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
反应混合物$→_{碳酸钠溶液}^{加入饱和}$$→_{苯甲醛}^{蒸馏除去}$$\stackrel{盐酸酸化}{→}$$\stackrel{操作I}{→}$$→_{干燥}^{过滤、洗涤}$肉桂酸晶体
(4)加饱和Na2CO3溶液除了转化醋酸,主要目的是将肉桂酸转化为肉桂酸钠,溶解于水.
(5)操作I是冷却结晶;若所得肉桂酸晶体中仍然有杂质,欲提高纯度可以进行的操作是重结晶(均填操作名称).
(6)设计实验方案检验产品中是否含有苯甲醛取样,加入银氨溶液共热,若有银镜出现,说明含有苯甲醛,或加入用新制氢氧化铜悬浊液,若出现砖红色沉淀,说明含有苯甲醛.
| A. | 制备Fe(OH)3胶体,通常是将FeCl3固体溶于热 NaOH溶液中 | |
| B. | 为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量 | |
| C. | 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 | |
| D. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |

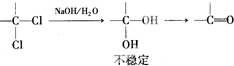

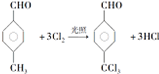 ,反应类型为取代反应
,反应类型为取代反应 +n
+n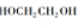 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$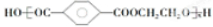 +(2n-1)H2O
+(2n-1)H2O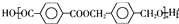 的路线流程图:
的路线流程图: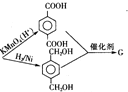 合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.