题目内容
10.下列有关实验的说法正确的是( )| A. | 制备Fe(OH)3胶体,通常是将FeCl3固体溶于热 NaOH溶液中 | |
| B. | 为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量 | |
| C. | 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 | |
| D. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |
分析 A.将FeCl3固体溶于热NaOH溶液中,生成沉淀;
B.瓷坩埚中的二氧化硅与熔化氢氧化钠反应;
C.Al与NaOH溶液反应,而Fe不能;
D.使澄清石灰水变浑浊的气体,为二氧化碳或二氧化硫.
解答 解:A.制备Fe(OH)3胶体,应将饱和FeCl3溶液滴加到沸水中,故A错误;
B.为测定熔融氢氧化钠的导电性,可在铁坩埚中熔化氢氧化钠固体后进行测量,故B错误;
C.Al与NaOH溶液反应,而Fe不能,则可加入过量的氢氧化钠溶液,完全反应后过滤可除杂,故C正确;
D.使澄清石灰水变浑浊的气体,为二氧化碳或二氧化硫,则原溶液中可能含CO32-或SO32-,或HCO3-等,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及胶体制备、物质的性质、混合物分离提纯、离子检验等,把握物质的性质、反应原理及实验技能为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
1.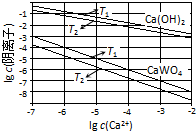 已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小.在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应Ⅰ:WO42-(aq)+Ca(OH)2(s)═CaWO4(s)+2OH-(aq).
已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小.在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应Ⅰ:WO42-(aq)+Ca(OH)2(s)═CaWO4(s)+2OH-(aq).
(1)图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线.
①计算T1时KSP(CaWO4)=1×10-10.
②T1< T2(填“>”“=”或“<”).
(2)反应Ⅰ的平衡常数K理论值如表:
①该反应平衡常数K的表达式为$\frac{{c}^{2}(O{H}^{-})}{c(W{{O}_{4}}^{2-})}$.
②该反应的△H>0(填“>”“=”或“<”).
③由于溶液中离子间的相互作用,实验测得的平衡常数与理论值相距甚远.50℃时,向一定体积的钨酸钠碱性溶液[c(Na2WO4)=c(NaOH)=0.5mol•L-1]中,加入过量Ca(OH)2,反应达到平衡后WO42-的沉淀率为60%,计算实验测得的平衡常数.
(3)制取钨酸钙时,适时向反应混合液中添加适量盐酸,分析其作用:加入盐酸,消耗反应生成的OH-,使溶液中OH-浓度减小,平衡向正反应方向移动,提高WO42-的沉淀率.
 已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小.在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应Ⅰ:WO42-(aq)+Ca(OH)2(s)═CaWO4(s)+2OH-(aq).
已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小.在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应Ⅰ:WO42-(aq)+Ca(OH)2(s)═CaWO4(s)+2OH-(aq).(1)图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线.
①计算T1时KSP(CaWO4)=1×10-10.
②T1< T2(填“>”“=”或“<”).
(2)反应Ⅰ的平衡常数K理论值如表:
| 温度/℃ | 25 | 50 | 90 | 100 |
| K | 79.96 | 208.06 | 222.88 | 258.05 |
②该反应的△H>0(填“>”“=”或“<”).
③由于溶液中离子间的相互作用,实验测得的平衡常数与理论值相距甚远.50℃时,向一定体积的钨酸钠碱性溶液[c(Na2WO4)=c(NaOH)=0.5mol•L-1]中,加入过量Ca(OH)2,反应达到平衡后WO42-的沉淀率为60%,计算实验测得的平衡常数.
(3)制取钨酸钙时,适时向反应混合液中添加适量盐酸,分析其作用:加入盐酸,消耗反应生成的OH-,使溶液中OH-浓度减小,平衡向正反应方向移动,提高WO42-的沉淀率.
18. 模拟侯氏制碱法原理,在CaCl2浓溶液中通入NH3和CO2可制得纳米级材料,装置见图示.下列说法正确的是( )
模拟侯氏制碱法原理,在CaCl2浓溶液中通入NH3和CO2可制得纳米级材料,装置见图示.下列说法正确的是( )
 模拟侯氏制碱法原理,在CaCl2浓溶液中通入NH3和CO2可制得纳米级材料,装置见图示.下列说法正确的是( )
模拟侯氏制碱法原理,在CaCl2浓溶液中通入NH3和CO2可制得纳米级材料,装置见图示.下列说法正确的是( )| A. | a通入适量的CO2,b通入足量的NH3,纳米材料为Ca(HCO3)2 | |
| B. | a通入足量的NH3,b通入适量的CO2,纳米材料为Ca(HCO3)2 | |
| C. | a通入适量的CO2,b通入足量的NH3,纳米材料为CaCO3 | |
| D. | a通入少量的NH3,b通入足量的CO2,纳米材料为CaCO3 |
15.下列变化属于物理变化的是( )
| A. | 氧气在放电条件下变成臭氧 | B. | 加热胆矾成白色无水硫酸铜 | ||
| C. | 漂白的草帽久置空气中变黄 | D. | 氢氧化铁胶体加入硫酸镁产生沉淀 |
19.下列说法中一定不正确的是( )
| A. | 某原子K层上只有一个电子 | |
| B. | 某离子L层和M层上的电子数均为K层的4倍 | |
| C. | 某离子M层上的电子数为L层上的4倍 | |
| D. | 某离子的核电荷数与最外层电子数相等 |
20.下列装置或操作能达到实验目的(必要的夹持装置及石棉网已省略)的是( )
| A. |  石油蒸馏 | B. |  实验室用乙醇制取乙烯 | ||
| C. |  实验室制取乙酸乙酯 | D. |  证明酸性:盐酸>碳酸>苯酚 |
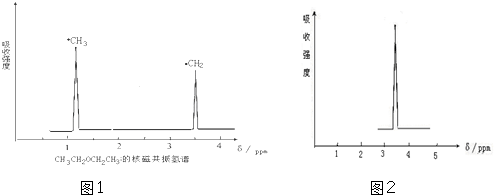
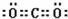 ;
;