题目内容
5. 如图为某品牌酱油标签的一部分:
如图为某品牌酱油标签的一部分:(1)氨基酸态氮的含量是酱油质量的重要指标,这些氨基酸是由大豆中的主要营养物质蛋白质水解而来的.
(2)配料清单中属于防腐剂的是苯甲酸钠.
(3)小麦中的主要营养物质是淀粉,写出这种物质完全水解的化学方程式:(C6H10O5)n+n H2O$\stackrel{催化剂}{→}$n C6H12O6.
分析 (1)蛋白质水解生成氨基酸;
(2)苯甲酸钠是应用很广的化学防腐剂,在酸性环境下能抑制微生物生长;
(3)小麦中的主要营养物质是淀粉,淀粉水解生成葡萄糖.
解答 解:(1)大豆富含蛋白质,蛋白质水解生成氨基酸,故答案为:蛋白质;
(2)苯甲酸钠又名安息香酸钠,亲油性较大,易穿透细胞膜进入细胞体内,干扰细胞膜的通透性,抑制细胞膜对氨基酸的吸收;苯甲酸钠进入细胞体内电离酸化细胞内的碱储,并抑制细胞的呼吸酶系的活性,从而起到食品防腐的目的,是常用的食品防腐剂,故答案为:苯甲酸钠;
(3)小麦中的主要营养物质是淀粉;完全水解的化学方程式:(C6H10O5)n+n H2O$\stackrel{催化剂}{→}$n C6H12O6,故答案为:淀粉;(C6H10O5)n+n H2O$\stackrel{催化剂}{→}$n C6H12O6.
点评 本题考查化学与生活,涉及蛋白质水解、食品防腐剂苯甲酸钠、小麦中的主要营养物质、铁强化酱油等知识,侧重基础知识的考查,平时注意化学与生活知识的积累,题目难度不大.

练习册系列答案
相关题目
13.硫酸、硝酸都是重要的化工原料,下列实验事实与浓硫酸或硝酸性质不相对应的一组是( )
| A. | 用铝槽车盛运浓硫酸--强氧化性 | |
| B. | 久置浓硝酸变黄--不稳定性 | |
| C. | 浓硫酸能使蔗糖变黑并膨胀--吸水性 | |
| D. | 用稀硝酸洗涤做过银镜反应的试管--强氧化性和酸性 |
20.与50mL 0.1molL-1 Na2CO3 溶液中 Na+ 的物质的量浓度相同的溶液是( )
| A. | 50mL 0.2mol•L-1 的NaCl溶液 | |
| B. | 100mL 0.05mol•L-1 的NaCl溶液 | |
| C. | 25mL 0.2mol•L-1 的Na2SO4溶液 | |
| D. | 1.06g Na2CO3固体溶于水配成 100mL溶液 |
10.设反应C+CO2?2CO(正反应吸热)反应速率为v1,N2+3H2?2NH3(正反应放热),反应速率为v2.对于上述反应,当温度升高时,v1、v2的变化情况为( )
| A. | 同时增大 | B. | 同时减小 | C. | v1增大,v2减小 | D. | v1减小,v2增大 |
17.“类推”是一种在化学学习中常用的方法,下列类推结论中正确的是( )
| A. | Al在氧气中生成Al2O3,Fe在氧气中也生成Fe2O3 | |
| B. | 第VA族氢化物的熔沸点顺序是NH3>AsH3>PH3;则第 VIA族氢化物的熔沸点顺序也是H2O>H2Se>H2S | |
| C. | 工业上用电解熔融的氯化镁制备镁单质,工业上也可用电解熔融的氯化铝制备铝单质 | |
| D. | BaCl2溶液中通入SO2无沉淀产生,则Ba(NO3)2溶液中通入SO2也无沉淀产生 |
14.等体积、等物质的量浓度的盐酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为2:3,则甲、乙两烧杯中的反应情况可能分别是( )
| A. | 甲、乙中都是铝过量 | B. | 甲中铝过量、乙中碱过量 | ||
| C. | 甲中酸过量、乙中铝过量 | D. | 甲中酸过量、乙中碱过量 |
15.某同学想用实验证明FeCl3溶液显黄色不是Cl-造成的,下列实验中无意义的是( )
| A. | 观察KCl溶液没有颜色 | |
| B. | 加水稀释后FeCl3溶液黄色变浅 | |
| C. | 向FeCl3溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失 | |
| D. | 向FeCl3溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液黄色消失 |
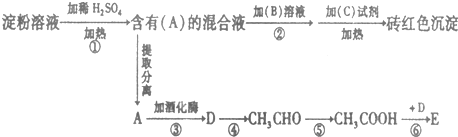
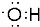 ;
;