题目内容
6.某有机物在O2中充分燃烧生成CO2和H2O的物质的量之比为1:2,由此可得出的结论是( )| A. | 该有机物分子中C、H、O原子个数比为1:4:1 | |
| B. | 该有机物分子中C、H原子个数比为1:4 | |
| C. | 该有机物中必定含有氧元素 | |
| D. | 该有机物化学式为CH4O |
分析 有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1:2,则确定有机物分子中C、H个数之比为1:4,有机物可能是甲烷,也可能是含氧有机物.
解答 解:有机物在氧气中充分燃烧充分生成CO2和H2O的物质的量之比为1:2,根据原子守恒可知,原有机物中的C和H的物质的量之比为1:4,有机物可能是CH4,也可能是含氧有机物CH3OH,故B正确、ACD错误,故选B.
点评 本题考查有机物燃烧的计算,难度不大,注意利用原子守恒确定有机物分子中C、H原子个数之比,但不能确定是否含有氧元素.

练习册系列答案
相关题目
17.下列有关电解质溶液中粒子浓度关系正确的是( )
| A. | pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 | |
| B. | 含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-) | |
| C. | 0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| D. | 含等物质的量的NaHC2O4和Na2C2O4的溶液:2c(Na+)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
14.如图中表示外界条件(T、P)的变化对下列反应的影响L(s)+G(g)?2R(g);△H>0,y轴表示的是( )
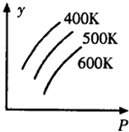

| A. | 平衡时,混合气体中R的百分含量 | B. | 平衡时,混合气中G的百分含量 | ||
| C. | G的转化率 | D. | L的转化率 |
11.下列各项操作错误的是?( )
| A. | 为保证分液漏斗内的液体顺利流出,需将上面的塞子拿下 | |
| B. | 进行分液时,分液漏斗中的下层液体从下端流出,上层则从上口倒出 | |
| C. | 萃取、分液前需对分液漏斗时行检漏 | |
| D. | 用酒精萃取溴水中的碘单质的操作,可选用分液漏斗而后静置分液 |
18.下列判断正确的是( )
| A. | 根据同周期元素的第一电离能变化趋势,推出P的第一电离能比S大 | |
| B. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正化合价都是+7 | |
| C. | 晶体中一定存在化学键 | |
| D. | 正四面体分子中键角只能是109°28′ |
16.下列溶液,一定呈中性的是( )
| A. | c(H+)=1×10-7mol/L的溶液 | |
| B. | pH=pOH的溶液(pOH是OH-浓度的负对数) | |
| C. | pH=14-pOH的溶液 | |
| D. | 由等体积、等物质的量浓度的一元酸跟氢氧化钠溶液混合后所形成的溶液 |