题目内容
9.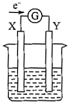 如图所示的原电池装置,X、Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列说法正确的是( )
如图所示的原电池装置,X、Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列说法正确的是( )| A. | 外电路的电流方向为:X→外电路→Y | |
| B. | 若两电极分别为Zn和石墨棒,则X为石墨棒,Y为Zn | |
| C. | 若两电极都是金属,则它们的活动性为X>Y | |
| D. | X极上发生的是还原反应,Y极上发生的氧化反应 |
分析 原电池装置,X、Y为两个电极,电解质溶液为稀硫酸,由外电路中的电子流向可知,X为负极,Y为正极,结合负极发生氧化反应、负极金属活泼等来解答.
解答 解:由外电路中的电子流向可知,X为负极,Y为正极,
A.由图可知电子的流动方向是X→外电路→Y,则电流的方向应该为Y→外电路→X,故A错误;
B.X为原电池的负极,Y为正极,则X应为Zn,故B错误;
C.两个电极都是金属,X为负极,则X的活动性比Y强,故C正确;
D.X极上发生的是氧化反应,Y极上发生的是还原反应,故D错误;
故选C.
点评 本题考查原电池的工作原理,明确电子的流向判断正负极为解答的关键,侧重电子流向、电极判断及金属性比较、电极反应的考查,注重基础知识的训练,题目难度不大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案
相关题目
19.为除去括号内的少量杂质,所选用的试剂或方法不正确的是( )
| A. | Na2CO3溶液(NaHCO3),加入适量的NaOH溶液 | |
| B. | NaHCO3溶液(Na2CO3),通入过量的CO2气体 | |
| C. | CO2气体(HCl气体),通过饱和的Na2CO3溶液 | |
| D. | SiO2(H2SiO3),加热 |
20.晶胞是晶体结构中可重复出现的最小的结构单元,C60晶胞结构如图所示,下列说法正确的是( )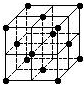

| A. | C60摩尔质量是720 | |
| B. | C60属于离子晶体 | |
| C. | 在C60晶胞中有14个C60分子 | |
| D. | 每个C60分子周围与它距离最近等距离的C60分子有12个 |
17.下列叙述正确的是( )
| A. | 1molH2O的质量为18g/mol | |
| B. | O2 的摩尔质量为32g | |
| C. | 2mol NaOH 溶于1 L水中配成溶液的浓度为2mol/L | |
| D. | 6.02×1023个CO分子的质量约为28g |
4.根据下列反应:①H2S+I2═S↓+2HI;②2FeCl3+2HI═2FeCl2+2HCl+I2;③2FeCl2+Cl2═2FeCl3,可以判断有关物质的氧化性由强到弱的顺序正确的是( )
| A. | Cl2>Fe3+>I2>S | B. | S>I2>Fe3+>Cl2 | C. | Fe3+>Cl2>H2S>I2 | D. | Cl2>I2>Fe3+>H2S |
1.下列物质发生变化时,所克服的粒子间相互作用属同种类型的是( )
| A. | 碘与干冰分别受热变为气体 | B. | 硝酸铵与硝酸分别受热变为气体 | ||
| C. | 氯化钠与氯化氢分别溶解在水中 | D. | 氧化铝与冰分别受热熔化 |
19.“绿色化学”是21世纪化学发展的主导方向,下列不符合“化学反应的绿色化学”的是( )
| A. | 消除硫酸厂尾气中的SO2:SO2+2NH3+H2O═(NH4)2SO3 | |
| B. | 消除制硝酸工业尾气中的氢氧化物:NO2+NO+2NaOH═2NaNO2+H2O | |
| C. | 制CuSO4:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O | |
| D. | 制CuSO4:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,CuO+H2SO4(稀)═CuSO4+H2O |
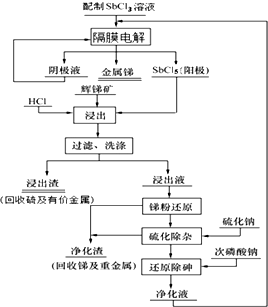 我国锑的蕴藏量占世界第一位.某课题组电解三氯化锑水溶液,利用阳极生成的五氯化锑作为浸出剂,对辉锑矿(Sb2S3)进行酸性浸出;从而实现浸出-电解的闭路循环,解决了传统炼锑过程中“工业三废”排放量大的问题.流程如图:
我国锑的蕴藏量占世界第一位.某课题组电解三氯化锑水溶液,利用阳极生成的五氯化锑作为浸出剂,对辉锑矿(Sb2S3)进行酸性浸出;从而实现浸出-电解的闭路循环,解决了传统炼锑过程中“工业三废”排放量大的问题.流程如图: A、B、C是单质,其中A是常见的活泼金属,B和C都是无色气体,丁加热后可生成甲.各种物质间的转化关系如图:
A、B、C是单质,其中A是常见的活泼金属,B和C都是无色气体,丁加热后可生成甲.各种物质间的转化关系如图: