题目内容
稀氨水中存在下述平衡: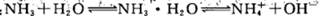 改变下列条件,能使电离程度增大的是
改变下列条件,能使电离程度增大的是
| A.加浓氨水 | B.升高温度 | C.加NH4Cl溶液 | D.加NaOH溶液 |
B
解析试题分析:A、加浓氨水,电离平衡正向移动,但一水合氨的电离程度减小,错误;B、弱电解质的电离吸热,升高温度,平衡正向移动,电离程度增大,正确;C、向氨水中加入NH4Cl溶液,溶液中c(NH4+)增大,平衡逆向移动,电离程度减小,错误; D、向氨水中加入NaOH溶液,氢氧根离子浓度增大,电离平衡向逆反应方向移动,电离程度减小,错误。
考点:考查弱电解质电离平衡的影响因素。

练习册系列答案
相关题目
某温度下,向一定体积0.1 mol/L的氨水中逐滴滴加0.1mol/L的盐酸,溶液中pH与pOH[注:pOH=-lgc(OH-)]的变化关系如图所示,则下列说法中错误的是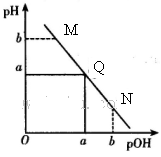
| A.M点所示溶液中c( NH4+)>c(Cl-) |
| B.Q点所示溶液的导电熊力强于M点 |
| C.Q点消耗盐酸的体积等于氨水的体积 |
| D.M点和N点所示溶液中水的电离程度相同 |
某温度下,pH相同的盐酸和氯化铵溶液分别稀释,pH随溶液体积变化的曲线如下图所示。据图判断下列叙述中,正确的是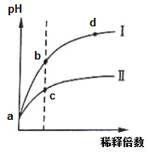
| A.Ⅰ为氯化铵稀释时pH值变化曲线,Ⅱ为盐酸稀释时pH值变化曲线 |
| B.b点溶液中水的电离程度比d点溶液中水的电离程度大,但两点的KW相同 |
| C.a点时,等体积的两溶液分别与NaOH反应,消耗的NaOH量相同 |
| D.c点溶液的导电能力一定比b点溶液导电能力强 |
0.1 mol/L K2CO3溶液中,若要使c(CO32-)更接近0.1 mol/L,可采取的措施是
| A.加入少量盐酸 | B.加KOH固体 | C.加水 | D.加热 |
实验:①0.1mol·L-1AgNO3溶液和0.1mol·L-1NaCl溶液等体积混合得到浊液a,过滤得到
滤液b和白色沉淀c;②向滤液b中滴加0.1mol·L-1KI溶液,出现浑浊;③向沉淀c中滴加0.1mol·L-1KI溶液,沉淀变为黄色。下列分析不正确的是:
A.浊液a中存在沉淀溶解平衡:AgCl(g) 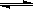 Ag+(aq)+Cl-(aq) Ag+(aq)+Cl-(aq) |
| B.滤液b中不含有Ag+ |
| C.③中颜色变化说明AgCl转化为AgI |
| D.实验可以证明AgI比AgCl更难溶 |
水中加入下列溶液对水的电离平衡不产生影响的是( )
| A.NaHSO4溶液 | B.KF溶液 | C.KAl(SO4)2溶液 | D.NaI溶液 |
下列叙述正确的是( )。
| A.在常温下,无论是纯水,还是酸性、碱性或中性稀溶液中,c(H+)·c(OH-)=1×10-14 |
| B.c(H+)=1×10-7 mol·L-1的溶液一定是中性溶液 |
| C.0.2 mol·L-1 CH3COOH溶液中的c(H+)是0.1 mol·L-1 CH3COOH溶液中的c(H+)的2倍 |
| D.任何浓度的溶液都可以用pH来表示其酸碱性的强弱 |
下列有关实验原理、方法和结论都正确的是( )
| A.用HNO2溶液做导电性实验,灯光较暗,说明HNO2是弱电解质 |
| B.在滴有酚酞的Na2CO3溶液中逐滴加入BaCl2溶液,红色逐渐褪去,说明Na2CO3溶液中存在水解平衡 |
| C.将等体积、等pH的盐酸和醋酸溶液分别稀释相同倍数,醋酸溶液的pH变化大 |
| D.利用溶解性的不同,可用酒精将碘水中的碘萃取出来 |