题目内容
10.在容积可变的密闭容器中存在如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)+Q(Q>0),下列对图象的分析中不正确的是( )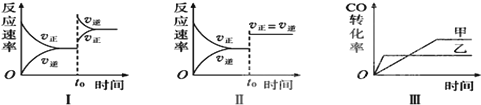
| A. | 图Ⅰ研究的是t0时升高温度对反应速率的影响 | |
| B. | 图Ⅱ研究的是t0时增大压强(缩小体积)或使用催化剂对反应速率的影响 | |
| C. | 图Ⅲ研究的是压强对化学平衡的影响,且乙压强大于甲 | |
| D. | 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 |
分析 A.图Ⅰ正逆反应速率均增大,且逆反应速率大于正反应速率,平衡向逆反应方向移动即升高温度;
B.图Ⅱ中正逆反应速率同等程度的增大即增大压强或者使用催化剂;
C.CO(g)+H2O(g)?CO2(g)+H2(g)+Q(Q>0),该反应为气体体积不变的放热反应,所以改变压强平衡不移动;
D.图Ⅲ中乙先达到平衡状态,且乙中CO的转化率小即为温度对平衡的影响.
解答 解:A.该反应放热,升高温度平衡向逆反应方向移动,图象符合,故A正确;
B.由于反应中反应前后气体的体积不变,则增大压强平衡不移动,催化剂只改变反应速率,不影响平衡移动,图象符合,故B正确;
C.由于反应中反应前后气体的体积不变,则增大压强平衡不移动,与图象不符合,故C错误;
D.该反应放热,升高温度平衡向逆反应方向移动,图中乙大于甲,CO的转化率降低,图象符合,故D正确;
故选C.
点评 本题考查化学平衡图象问题,题目难度中等,明确方程式的特征以及外界条件对平衡移动的影响是解答该题的关键,答题时注意把握图象曲线的变化趋势.

练习册系列答案
相关题目
20.下列描述中正确的是( )
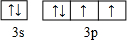
| A. | 氮原子的价电子排布图: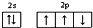 | |
| B. | 价电子排布为4s24p3的元素位于第四周期第VA族,是p区元素 | |
| C. | 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态 | |
| D. | 第一电离能和电负性:1s22s22p4>1s22s22p3 |
1.下列属于纯净物的是( )
| A. | 汽油 | B. | 煤 | C. | 乙烯 | D. | 石油裂解气 |
18.下列烃的含氧衍生物中,只能与金属钠反应,不与碳酸氢钠溶液反应的是( )
| A. | CH2=CHCHO | B. | 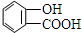 | C. | CH3COOCH3 | D. | 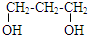 |
5.将铜片和石墨棒用导线相连(其间连有电流表),并同时插入Fe2(SO4)3溶液中,下列现象中不可能出现的是( )
| A. | 铜片质量减少 | B. | 石墨棒质量增加 | C. | 电流表指针偏转 | D. | 溶液显蓝色 |
2.某同学在实验报告中有以下的实验数据:
①用托盘天平称取11.7g食盐
②用量筒量取5.26mL盐酸
③用广泛pH试纸测得溶液的pH是3.5
④用标准NaOH溶液滴定未知浓度的盐酸,用去23.10mL NaOH溶液.
其中数据合理的是( )
①用托盘天平称取11.7g食盐
②用量筒量取5.26mL盐酸
③用广泛pH试纸测得溶液的pH是3.5
④用标准NaOH溶液滴定未知浓度的盐酸,用去23.10mL NaOH溶液.
其中数据合理的是( )
| A. | ①②③ | B. | ①③④ | C. | ①②③④ | D. | ①④ |
19.根据如表五种元素的第一至第四电离能数据(单位:kJ/mol),回答下面各题:
(1)在周期表中,最可能处于同一族的是E
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)下列离子的氧化性最弱的是D
A.S2+ B.R+ C.T3+ D.U+
(3)下列元素中,化学性质和物理性质最像Q元素的是C
A.硼 B.铍 C.氦 D.氢
(4)T元素最可能是p区元素,其氯化物的化学式为TCl3.
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)下列离子的氧化性最弱的是D
A.S2+ B.R+ C.T3+ D.U+
(3)下列元素中,化学性质和物理性质最像Q元素的是C
A.硼 B.铍 C.氦 D.氢
(4)T元素最可能是p区元素,其氯化物的化学式为TCl3.
20.下列物质中,不属于电解质的是( )
| A. | 乙醇 | B. | CH3COOH | C. | BaCl2 | D. | Cl2 |