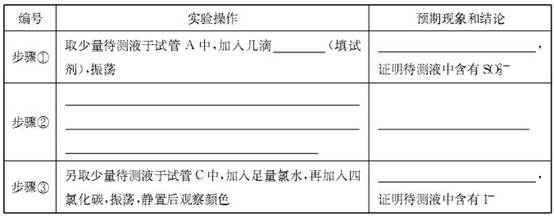
题目内容
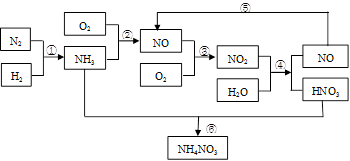
工业尾气中氮氧化物通常采用氨催化吸收法,其原理是NH3与NOx在催化剂作用下反应生成无毒的物质。某校活动小组同学采用以下装置和步骤模拟工业上氮氧化物的处理过程。
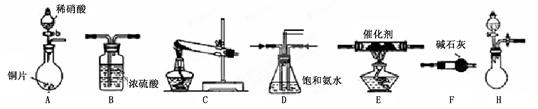
I.探究制取NH3的方法
(1)在上述装置中,H能快速、简便制取NH3,装置中需要添加的反应试剂为 。
(2)为探究更好的实验效果,活动小组同学采用上述C装置来制取氨气,在控制实验条件相同的情况下,获得下表中实验数据。
分析表中数据,你认为哪种方案制取氨气的效果最好 (填序号),从该方案选择的原料分析制气效果好的可能原因是 。
II.模拟尾气处理
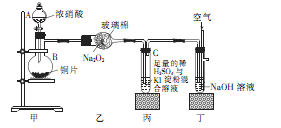
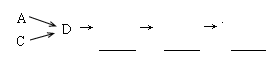
活动小组同学选用上述部分装置,按下列顺序连接成模拟尾气处理装置进行实验。
(1)请从上述装置中选择你认为合理的进行补充(所选装置不能重复)。
(2)A中反应的离子方程式为 。
(3)D装置的作用有:使气体混合均匀、调节气流速度、 。
(4)D装置中的液体还可换成 (填序号)。
a.H2O b.CCl4 c.浓H2SO4 d.CuSO4溶液
(5)该小组同学所设计的模拟尾气处理装置中还存在一处明显的缺陷是 。

I.探究制取NH3的方法
(1)在上述装置中,H能快速、简便制取NH3,装置中需要添加的反应试剂为 。
(2)为探究更好的实验效果,活动小组同学采用上述C装置来制取氨气,在控制实验条件相同的情况下,获得下表中实验数据。
| 试剂组合序号 | 固体试剂 | NH3体积(mL) | |
| a | 6.0 g Ca(OH)2(过量) | 5.4 g NH4Cl | 1344 |
| b | 5.4g (NH4)2SO4 | 1364 | |
| c | 6.0 g NaOH(过量) | 5.4 g NH4Cl | 1568 |
| d | 5.4g (NH4)2SO4 | 1559 | |
| e | 6.0 g CaO(过量) | 5.4 g NH4Cl | 1753 |
| f | 5.4 g (NH4)2SO4 | 1792 | |
分析表中数据,你认为哪种方案制取氨气的效果最好 (填序号),从该方案选择的原料分析制气效果好的可能原因是 。
II.模拟尾气处理
活动小组同学选用上述部分装置,按下列顺序连接成模拟尾气处理装置进行实验。
(1)请从上述装置中选择你认为合理的进行补充(所选装置不能重复)。

(2)A中反应的离子方程式为 。
(3)D装置的作用有:使气体混合均匀、调节气流速度、 。
(4)D装置中的液体还可换成 (填序号)。
a.H2O b.CCl4 c.浓H2SO4 d.CuSO4溶液
(5)该小组同学所设计的模拟尾气处理装置中还存在一处明显的缺陷是 。
I.(1)生石灰与浓氨水(或烧碱与浓氨水) (答化学式给分)(2分)
(2)f (2分) (NH4)2SO4受热不分解,CaO又有吸水作用(合理答案均给分)(2分)
II.(1)F E B (2分)
(2)3Cu + 2NO3-+8H+ 3Cu2+ + 2NO↑ +4H2O (2分)
3Cu2+ + 2NO↑ +4H2O (2分)
(3)防止氨气溶解(或防止倒吸)(2分)
(4)b(2分)
(5)未反应的NO无法处理,会污染环境 (2分)
(2)f (2分) (NH4)2SO4受热不分解,CaO又有吸水作用(合理答案均给分)(2分)
II.(1)F E B (2分)
(2)3Cu + 2NO3-+8H+
 3Cu2+ + 2NO↑ +4H2O (2分)
3Cu2+ + 2NO↑ +4H2O (2分)(3)防止氨气溶解(或防止倒吸)(2分)
(4)b(2分)
(5)未反应的NO无法处理,会污染环境 (2分)
试题分析:(1)依据装置分析制备氨气气体是利用液体通过分液漏斗滴入烧瓶中不加热进行的反应,实验目的是制取、干燥和收集氨气的装置,制备氨气先干燥再收集,氨气比空气轻,应用向下排气法收集;制备氨气可以利用浓氨水滴入氧化钙或固体氢氧化钠或碱石灰,溶解放热时一水合氨分解生成氨气;
(2)因为NH4Cl受热易分解,生成的部分NH3和HCl又重新结合成NH4Cl,而用NaOH或Ca(OH)2作反应物产生的水较多,吸收的NH3较多,由表中数据可以看出,f制NH3产率最高;
II.(1)混合气体干燥后进入反应装置,然后用浓硫酸吸收没有反应的氨气。
(2)稀硝酸具有强氧化性,与铜发生氧化还原反应生成硝酸铜和NO等,反应的离子方程式为3Cu + 2NO3-+8H+
 3Cu2+ + 2NO↑ +4H2O;
3Cu2+ + 2NO↑ +4H2O;(3)D装置使气体混合均匀、调节气流速度,另外,氨气难溶于饱和氨水,可防止倒吸;
(4)氨气可溶于硫酸铜溶液、水以及硫酸中,可产生倒吸,氨气为极性分子,不溶于非极性溶剂,可用CCl4代替饱和氨水;
(5)缺少尾气处理装置,过量的NO会污染空气。

练习册系列答案
相关题目
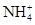
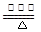 ____NO+ ________
____NO+ ________ 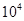 L(标准状况)该尾气需42.5gNH3,则x= _ 。
L(标准状况)该尾气需42.5gNH3,则x= _ 。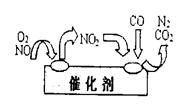
 7N2+12H2O(NO也有类似的反应)
7N2+12H2O(NO也有类似的反应)