题目内容
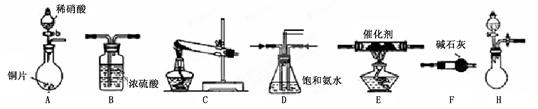
工业上利用氨催化氧化后,经过一系列反应可以制备硝酸。
(1)氨气催化氧化的化学方程式为 _
(2)某工厂排出的尾气中NOx的含量为0.56%(体积分数),用氨气可以将其转化为无害气体,发生的反应为:6NOx+4xNH3=(3+2x)N2+6xH2O 若处理1×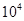 L(标准状况)该尾气需42.5gNH3,则x= _ 。
L(标准状况)该尾气需42.5gNH3,则x= _ 。
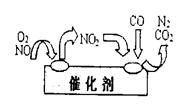
(3)NO和CO都是汽车尾气中的有害物质,必须进行处理。为避免污染,常给汽车安装尾气净化装置。净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如图所示。写出净化过程中的总化学反应方程式: 。
(1)氨气催化氧化的化学方程式为 _
(2)某工厂排出的尾气中NOx的含量为0.56%(体积分数),用氨气可以将其转化为无害气体,发生的反应为:6NOx+4xNH3=(3+2x)N2+6xH2O 若处理1×
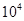 L(标准状况)该尾气需42.5gNH3,则x= _ 。
L(标准状况)该尾气需42.5gNH3,则x= _ 。(3)NO和CO都是汽车尾气中的有害物质,必须进行处理。为避免污染,常给汽车安装尾气净化装置。净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如图所示。写出净化过程中的总化学反应方程式: 。

(1)4NH3+5O2 =" 4NO" +6H2O (条件:加热,催化剂)
(2)1.5 (3)2NO+O2+4CO 4CO2+N2
4CO2+N2
(2)1.5 (3)2NO+O2+4CO
 4CO2+N2
4CO2+N2试题分析:(1)氨气催化氧化的化学方程式为4NH3+5O2 ="4NO" +6H2O
(2)1×104L尾气中NOx的体积为:1×104L×0.56%=56L,标准状况下NOx的物质的量为56L/22.4L/mol=2.5mol,42.5gNH3的物质的量为42.5g/17g/mol=2.5mol,
物质的量之比等于化学计量数之比,所以2.5mol:2.5mol=6:4x,解得x=1.5;
(3)NO2为中间产物,反应物为NO、O2、CO,产物为CO2、N2,反应方程式为2NO+O2+4CO
 4CO2+N2;
4CO2+N2;
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
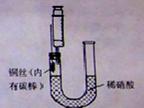
 N2O4(g) △H <0;N2O4为无色气体。
N2O4(g) △H <0;N2O4为无色气体。