题目内容
【题目】工业上常用铁质容器盛装冷浓硫酸。某学习小组为研究铁质材料与热浓硫酸的反应,设计了以下探究活动:
称取铁钉(碳素钢)6.0 g放入15.0 mL浓硫酸中,加热,充分应后得到溶液M并收集到气体N。
(1)该小组通过认真分析,认为M溶液中既含有Fe3+,也可能含有Fe2+。若确认溶液中有无Fe2+,应加入的试剂是___________(选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.NaOH溶液 d.酸性KMnO4溶液
(2)取320 mL(标准状况)气体N通入足量溴水中,然后加入足量BaCl2溶液,经过____________ 、______________(填操作名称)、干燥后,得到固体2.33 g。气体N与溴水反应的化学方程式为_______________,计算推知气体N中SO2的体积分数为_______________。
(3)该小组通过对铁钉的成分和SO2体积分数的分析,认为气体N中还可能含有H2和另外一种气体Q。你认为Q应该是_____________,理由是________________(用化学方程式表示)。
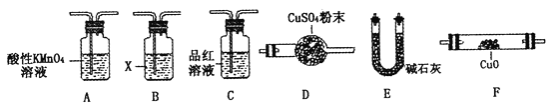
(4)取一定量N,利用下列仪器设计一个能同时检验N中含有H2和气体Q的装置(夹持仪器、橡胶管和加热装置省略),仪器的连接顺序是_____________(填字母),其中A的作用是_____________,B中试剂X的化学式是_____________________。
【答案】d 过滤 洗涤 SO2+Br2+2H2O=H2SO4+2HBr 70% CO2 C + 2H2SO4 (浓)![]() 2SO2↑+ CO2↑+ 2H2O A-C-B-E-F-D(或A-C-B-E-F-D-E) 除去N中的SO2, Ca(OH)2 或Ba(OH)2
2SO2↑+ CO2↑+ 2H2O A-C-B-E-F-D(或A-C-B-E-F-D-E) 除去N中的SO2, Ca(OH)2 或Ba(OH)2
【解析】
(1)Fe+2Fe3+=3Fe2+,+2价亚铁离子能使酸化的高锰酸钾褪色,溶液中已经有+3价铁离子,选择a会造成干扰,选b只能检验溶液中含有+3价铁离子,选c会造成两种沉淀,受氢氧化铁颜色的影响无法辨别,只能选d,故答案为:d;
(2)SO2具有还原性,通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4,生成的硫酸遇到氯化钡会产生白色沉淀,可以先洗涤然后再过滤来获得纯净的硫酸钡沉淀,则n(混合气体)=![]() ≈0.014mol,
≈0.014mol,
SO2~BaSO41mol 233g
n 2.33g
n=0.01mol
则SO2的体积分数:![]() ×100%≈70%,故答案为:过滤;洗涤;SO2+Br2+2H2O=2HBr+H2SO4;70%;
×100%≈70%,故答案为:过滤;洗涤;SO2+Br2+2H2O=2HBr+H2SO4;70%;
(3)在反应的过程中,碳单质可以和浓硫酸反应生成二氧化碳、二氧化硫等气体,故答案为:CO2;C+2H2SO4(浓)![]() 2SO2↑+CO2↑+2H2O;
2SO2↑+CO2↑+2H2O;
(4)推断所的气体中可能含有二氧化碳,结合图中设计装置的目的,可知检验二氧化碳的方法是首先将二氧化硫除去→确认二氧化硫已经完全除去→澄清石灰水,对于氢气的检验则可通过与灼热氧化铜的反应现象和对产物水的验证来实现,验证气体存在的顺序为:SO2→CO2→CO和H2被氧化→H2O→CO2,实验中要避免其它物质的性质干扰,顺序为:A-C-B-E-F-D(或A-C-B-E-F-D-E),其中A酸性高锰酸钾溶液的作用是除去二氧化碳中的SO2,B中试剂X的作用是除去二氧化硫,可以用Ca(OH)2或Ba(OH)2,
故答案为:A-C-B-E-F-D(或A-C-B-E-F-D-E);除去N中的SO2;Ca(OH)2或Ba(OH)2.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案