题目内容
11.下列各组元素中,属于同一周期的是( )| A. | Na、Li | B. | N、Cl | C. | Si、S | D. | O、P |
分析 原子结构中,具有相同电子层的原子,在同一周期,以此来解答.
解答 解:A.Na、Li分别在第三周期、第二周期,故A不选;
B.N、Cl分别在第二周期、第三周期,故B不选;
C.Si、S的原子结构中均有3个电子层,均位于第三周期,故C选;
D.O、P分别在第二周期、第三周期,故D不选;
故选C.
点评 本题考查元素周期表的结构及应用,为高频考点,侧重元素位置的考查,注意把握原子的电子层数等于周期数的关系,熟悉常见元素的位置即可解答,题目难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案
相关题目
1.汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KN03→K20+5Na20+16N2↑.若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
| A. | 生成40.0 L N2(标准状况) | |
| B. | 有0.250 mol KN03被氧化 | |
| C. | 转移电子的物质的量为1.25 mol | |
| D. | 被氧化的N原子的物质的量为2.5mol |
2.X、Y、Z、M、R、Q是短周期主族元素,部分信息如表所示:
(1)R在元素周期表中的位置是第三周期ⅦA族;
(2)Z的单质与水反应的化学方程式是2Na+2H2O=2NaOH+H2↑.
(3)Y与R相比,R非金属性较强,从原子结构角度解释原因:同周期自左而右,原子半径逐渐减小,得电子能力增强,非金属性增强,则非金属性Cl>Si;从实验事实角度解释,下列事实能证明这一结论的是bc(选填字母序号).
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性XR>YX4
c.Y与R形成的化合物中Y呈正价
d.将XR水溶液滴入Z2YM3溶液产生胶体
(4)根据表中数据推测,Y的原子半径的最小取值范围是大于0.099nm小于0.143nm.
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其它 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(2)Z的单质与水反应的化学方程式是2Na+2H2O=2NaOH+H2↑.
(3)Y与R相比,R非金属性较强,从原子结构角度解释原因:同周期自左而右,原子半径逐渐减小,得电子能力增强,非金属性增强,则非金属性Cl>Si;从实验事实角度解释,下列事实能证明这一结论的是bc(选填字母序号).
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性XR>YX4
c.Y与R形成的化合物中Y呈正价
d.将XR水溶液滴入Z2YM3溶液产生胶体
(4)根据表中数据推测,Y的原子半径的最小取值范围是大于0.099nm小于0.143nm.
6.如表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最稳定的是Ar(填元素符号).最活泼的金属是K(填元素符号),离子结构示意图为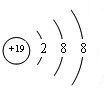 .元素⑩名称为溴,在周期表中的位置是第四周期ⅦA族.
.元素⑩名称为溴,在周期表中的位置是第四周期ⅦA族.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4.
(3)这些元素中能形成两性氢氧化物的元素是铝(填名称),写出该元素的氢氧化物与④的最高价氧化物的水化物反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(4)元素①、②的最简单氢化物的稳定性:H2O大于NH3.(填写氢化物的分子式)
(5)请设计一个实验方案,比较⑥、⑦单质氧化性的强弱:在Na2S溶液中滴加Cl2水,若溶液出现浑浊,说明Cl2的氧化性比S强.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .元素⑩名称为溴,在周期表中的位置是第四周期ⅦA族.
.元素⑩名称为溴,在周期表中的位置是第四周期ⅦA族.(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4.
(3)这些元素中能形成两性氢氧化物的元素是铝(填名称),写出该元素的氢氧化物与④的最高价氧化物的水化物反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(4)元素①、②的最简单氢化物的稳定性:H2O大于NH3.(填写氢化物的分子式)
(5)请设计一个实验方案,比较⑥、⑦单质氧化性的强弱:在Na2S溶液中滴加Cl2水,若溶液出现浑浊,说明Cl2的氧化性比S强.
3.铅的冶炼大致过程如下:①富集:将方铅矿(PbS)进行浮选;②焙烧:2PbS+3O2$\frac{\underline{\;高温\;}}{\;}$2PbO+2SO2;③制粗铅:PbO+C$\frac{\underline{\;高温\;}}{\;}$Pb+CO;PbO+CO$\frac{\underline{\;高温\;}}{\;}$Pb+CO2.下列说法正确的是( )
| A. | 浮选法富集方铅矿的过程属于化学变化 | |
| B. | 方铅矿焙烧反应中,PbS是还原剂,还原产物只有PbO | |
| C. | 将1molPbS冶炼成Pb理论上至少需要6g碳 | |
| D. | 整个冶炼过程中,制取1molPb共转移2mol电子 |
20.密闭容器中的可逆反应3A(g)?3B+C,△H=+890kJ/mol(A的式量为120)随着温度升高,容器中气体平均相对分子质量减小,则下列判断正确的是( )
| A. | 若C为固体,则B一定是气体 | |
| B. | B和C一定都是气体 | |
| C. | 若起始时往容器中投入18gA,则反应吸收的热量为44.5kJ | |
| D. | 若起始时往容器中投入18gA,则反应放出的热量为44.5kJ |