题目内容
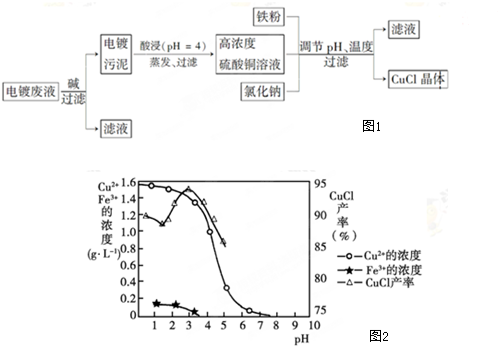
15.某学校化学课外活动小组的同学用粗铜(含杂质铁)按如下流程回收氯化铜晶体(CuCl2•2H2O)等相关物质.请回答下列问题:
(1)为得到固体Ⅰ,同学们设计如图装置:

①整盘装置有不足之处,要完成实验必须改进的是在A、C两处添加酒精灯.
②写出A中发生反应的离子方程式MnO2 +4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
③若进入装置C为纯净的氯气,需对装置做怎样处理?在A、B之间添加盛有饱和氯化钠溶液的洗气瓶.
(2)操作Ⅱ中所需的主要玻璃仪器有烧杯、玻璃棒、漏斗.
(3)试剂X为CuO或Cu(OH)2.
(4)由溶液IV获得CuCl2•2H2O晶体过程中,有同学发现溶液颜色由蓝色变为绿色进而变成黄绿色,经查阅资料发现氯化铜溶液中存在以下平衡关系:
[Cu(H2O)4]2+(aq)+4Cl-(aq)?[CuCl4]2-(aq)+4H2O(l)
(蓝色) (黄色)
①反应的化学平衡常数表达式K=$\frac{c(CuC{{l}_{4}}^{2-})}{c[Cu({H}_{2}O{)_{4}}^{2-}]•{c}^{4}(C{l}^{-})}$.
②当氯化铜溶液颜色由蓝色转变为黄绿色过程中,K值将不变(填“增大”、“不变”或“减小”).
③若在蒸发皿中直接加热溶液IV至蒸干,最后可能得到的物质为Cu(OH)2或CuO,请简述原因溶液中氯化铜发生水解:CuCl2+2H2O?Cu(OH)2+2HCl,加热HCl挥发,使平衡向生成氢氧化铜的方向进行,氢氧化铜受热分解得到CuO.
(5)为得到纯净的固体VI需要进行操作V(过滤、洗涤和烘干),请简述检验洗涤是否干净的操作步驟取少许洗涤液与试管中,滴加硝酸酸化的硝酸银溶液,若溶液变浑浊,说明没有洗涤干净,若无明显现象,说明洗涤干净.
分析 粗铜与氯气反应得到固体I为CuCl2,含有杂质铁与氯气反应得到FeCl3,再用盐酸溶解,过滤得到溶液中含有CuCl2、FeCl3,加入试剂X调节溶液pH,使溶液中Fe3+转化为Fe(OH)3沉淀,过滤除去,固体Ⅵ为Fe(OH)3,试剂X可以为CuO、Cu(OH)2,溶液Ⅳ为氯化铜溶液,再经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等得到氯化铜晶体.
(1)用装置A制备氯气,制备B干燥氯气,装置C为粗铜与氯气反应,A、C两处需要用酒精灯加热,D装置吸收未反应的氯气,防止污染空气.而盐酸易挥发,A装置中制备的氯气中利用HCl,应在A、B之间添加盛有饱和氯化钠溶液的洗气瓶,除去氯气的HCl;
(2)操作Ⅱ为过滤,用到的仪器有:烧杯、玻璃棒、漏斗、铁架台等;
(3)加入试剂X调节溶液pH,使溶液中Fe3+转化为Fe(OH)3沉淀,过滤除去,注意不能移入新杂质;
(4)①平衡常数为生成物浓度系数次幂之积与反应物浓度系数次之积的比值,水溶液中不需要标出水;
②平衡常数只受温度影响;
③溶液中氯化铜发生水解,加热HCl挥发,时水解平衡向生成氢氧化铜的方向进行,氢氧化铜受热分解得到CuO;
(5)固体VI的表面可能附着氯化铜,可以利用硝酸酸化的硝酸银溶液检验洗涤液中是否含有氯离子进行判断.
解答 解:粗铜与氯气反应得到固体I为CuCl2,含有杂质铁与氯气反应得到FeCl3,再用盐酸溶解,过滤得到溶液中含有CuCl2、FeCl3,加入试剂X调节溶液pH,使溶液中Fe3+转化为Fe(OH)3沉淀,过滤除去,固体Ⅵ为Fe(OH)3,试剂X可以为CuO、Cu(OH)2,溶液Ⅳ为氯化铜溶液,再经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等得到氯化铜晶体.
(1)用装置A制备氯气,制备B干燥氯气,装置C为粗铜与氯气反应,A、C两处需要用酒精灯加热,D装置吸收未反应的氯气,防止污染空气.而盐酸易挥发,A装置中制备的氯气中利用HCl,应在A、B之间添加盛有饱和氯化钠溶液的洗气瓶,除去氯气的HCl.
①制备氯气、粗铜与氯气反应均需要加热,要完成实验必须在A、C两处添加酒精灯,
故答案为:在A、C两处添加酒精灯;
②A中用二氧化锰与浓盐酸制备氯气,发生反应的离子方程式为:MnO2 +4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:MnO2 +4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
③盐酸易挥发,A装置中制备的氯气中利用HCl,应在A、B之间添加盛有饱和氯化钠溶液的洗气瓶,除去氯气的HCl,
故答案为:在A、B之间添加盛有饱和氯化钠溶液的洗气瓶;
(2)操作Ⅱ为过滤,用到的仪器有:烧杯、玻璃棒、漏斗、铁架台等,
故答案为:烧杯、玻璃棒、漏斗;
(3)加入试剂X调节溶液pH,使溶液中Fe3+转化为Fe(OH)3沉淀,过滤除去,注意不能移入新杂质,试剂X可以为CuO或Cu(OH)2等,
故答案为:CuO或Cu(OH)2;
(4)①反应[Cu(H2O)4]2+(aq)+4Cl-(aq)?[CuCl4]2-(aq)+4H2O的化学平衡常数表达式K=$\frac{c(CuC{{l}_{4}}^{2-})}{c[Cu({H}_{2}O{)_{4}}^{2-}]•{c}^{4}(C{l}^{-})}$,
故答案为:$\frac{c(CuC{{l}_{4}}^{2-})}{c[Cu({H}_{2}O{)_{4}}^{2-}]•{c}^{4}(C{l}^{-})}$;
②平衡常数只受温度影响,与离子浓度无关,温度不变,平衡常数不变,
故答案为:不变;
③溶液中氯化铜发生水解:CuCl2+2H2O?Cu(OH)2+2HCl,加热HCl挥发,使平衡向生成氢氧化铜的方向进行,氢氧化铜受热分解得到CuO,故最后可能得到的物质可能为Cu(OH)2或CuO,
故答案为:Cu(OH)2或CuO;溶液中氯化铜发生水解:CuCl2+2H2O?Cu(OH)2+2HCl,加热HCl挥发,使平衡向生成氢氧化铜的方向进行,氢氧化铜受热分解得到CuO;
(5)固体VI的表面可能附着氯化铜,可以利用硝酸酸化的硝酸银溶液检验洗涤液中是否含有氯离子,具体方案为:取少许洗涤液与试管中,滴加硝酸酸化的硝酸银溶液,若溶液变浑浊,说明没有洗涤干净,若无明显现象,说明洗涤干净,
故答案为:取少许洗涤液与试管中,滴加硝酸酸化的硝酸银溶液,若溶液变浑浊,说明没有洗涤干净,若无明显现象,说明洗涤干净.
点评 本题考查物质制备实验方案,涉及化学工艺流程、对装置分析评价、试剂选择、平衡常数、盐类水解、离子检验等,是对学生综合能力的考查,需要学生具备扎实的基础,难度中等.

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案| A. | 42 | B. | 39 | C. | 31 | D. | 28 |
| A. | 向Fe(NO3)2稀溶液中加入盐酸:Fe2++2H+═3Fe2++H2↑ | |
| B. | 铜片放入稀硝酸中:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| C. | 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH-═NH3↑+H2O | |
| D. | AlCl3溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |

| A. | 气态氢化物稳定性:R>Q | |
| B. | 元素T的离子半径>元素R的离子半径 | |
| C. | 与w同主族的某元素形成的18电子的氢化物分子中既有极性键又有非极性键 | |
| D. | Q可形成多种含氧酸 |
| 表述Ⅰ | 表述Ⅱ | |
| A | 在水中,NaCl的溶解度比I2的溶解度大 | NaCl晶体中C1-与Na+间的作用力大于碘晶体中分子间的作用力 |
| B | 通常条件下,CH4分子比PbH4分子稳定性高 | Pb的原子半径比C的大,Pb与H之间的键能比C与H间的小 |
| C | NaCl的熔点比MgO的熔点高 | NaCl的晶格能比MgO的晶格能大 |
| D | P4O10、C6H12O6溶于水后均不导电 | P4O10、C6H12O6均属于共价化合物 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 熔点:CO2>KCl>SiO2 | |
| B. | 酸性:HClO4>H2SO4>H3PO4 | |
| C. | 与同浓度的稀盐酸反应剧烈程度:Mg>Al | |
| D. | 热稳定性:HF>H2O>NH3 |