题目内容
18.由反应:2FeCl3+Cu→2FeCl2+CuCl2 推断出的氧化性或还原性强弱的结论,正确的是( )| A. | 氧化性 Cu2+>Fe2+ | B. | 氧化性 Fe3+>Cu2+ | ||
| C. | 还原性 Fe2+>Cu | D. | 还原性 Fe>Cu |
分析 氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的还原性,根据反应判断.
解答 解:根据氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的还原性,则2FeCl3+Cu=2FeCl2+CuCl2 中氧化性:FeCl3>CuCl2,即Fe3+>Cu2+,还原性:Cu>FeCl2,即Cu>Fe2+;
故选B.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重于基本概念的考查,题目难度不大

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.醋酸的下列性质中,可以证明它是弱电解质的是( )
| A. | 1mol•L-1的醋酸溶液中c(H+)=0.01mol•L-1 | |
| B. | 醋酸以任意比与H2O互溶 | |
| C. | 10mL 1mol•L-1的醋酸溶液恰好与10mL 1mol•L-1的NaOH溶液完全反应 | |
| D. | 醋酸溶液的导电性比盐酸弱 |
6.已知反应Cl2+H2O═HCl+HClO,对该反应的说法正确的是( )
| A. | Cl2是氧化剂,H2O是还原剂 | |
| B. | 氧化剂与还原剂的物质的量之比是1:2 | |
| C. | 按照化学方程式进行,氧化剂失电子1 mol | |
| D. | Cl2既是氧化剂又是还原剂 |
13.向含有KBr、NaI的混合溶液中通入过量的Cl2充分反应后,将溶液蒸干并进行灼烧,最后所得的固体物质是( )
| A. | NaCl和KCl | B. | KCl和NaBr | C. | NaCl和KI | D. | NaCl、KCl和I2 |
3.30mL0.1mol•L-1的Na2SO3溶液恰好将2×10-3molXO4-还原,则在还原产物中,X元素的化合价是( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
10.某种药物合成中间体结构简式为: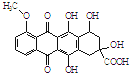 ,有关该物质的说法不正确的是( )
,有关该物质的说法不正确的是( )
 ,有关该物质的说法不正确的是( )
,有关该物质的说法不正确的是( )| A. | 属于芳香族化合物 | |
| B. | 能发生消去反应和酯化反应 | |
| C. | 1 mol该有机物与足量NaOH溶液反应,消耗5 mol NaOH | |
| D. | 能分别与金属Na、NaHCO3溶液反应 |
7. 氨作为一种富氢化合物,具有各种优点,特别是氨有着良好的产业基础,价格低廉,氨作为燃料电池燃料具有很大的发展潜力.氨氧燃料电池示意图,下列说法正确的是( )
氨作为一种富氢化合物,具有各种优点,特别是氨有着良好的产业基础,价格低廉,氨作为燃料电池燃料具有很大的发展潜力.氨氧燃料电池示意图,下列说法正确的是( )
 氨作为一种富氢化合物,具有各种优点,特别是氨有着良好的产业基础,价格低廉,氨作为燃料电池燃料具有很大的发展潜力.氨氧燃料电池示意图,下列说法正确的是( )
氨作为一种富氢化合物,具有各种优点,特别是氨有着良好的产业基础,价格低廉,氨作为燃料电池燃料具有很大的发展潜力.氨氧燃料电池示意图,下列说法正确的是( )| A. | NH3分子内可以形成氢键,故NH3很容易液化 | |
| B. | a电极的电极反应式为:NH3-5e-+5OH-═NO+4H2O | |
| C. | 正极消耗标准状况下空气2.24L时,电池中转移的电子数目为0.4NA | |
| D. | 反应过程中,K+向b极移动.一段时间后,电解质溶液的pH将减小 |