题目内容
6.已知反应Cl2+H2O═HCl+HClO,对该反应的说法正确的是( )| A. | Cl2是氧化剂,H2O是还原剂 | |
| B. | 氧化剂与还原剂的物质的量之比是1:2 | |
| C. | 按照化学方程式进行,氧化剂失电子1 mol | |
| D. | Cl2既是氧化剂又是还原剂 |
分析 Cl2+H2O═HCl+HClO中,Cl元素的化合价由0升高为+1价,Cl元素的化合价由于0降低为-1价,所以Cl2既是氧化剂又是还原剂,以此来解答.
解答 解:该反应中只有Cl元素的化合价变化,既升高又降低,则Cl2既是氧化剂又是还原剂,并且氧化剂与还原剂的物质的量之比是1:1,按照化学方程式进行,氧化剂得电子1 mol;而H2O既不是氧化剂也不是还原剂,
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注意从元素化合价角度分析,侧重氧化剂、还原剂判断的考查,题目较简单.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
16.A、B、C三种强电解质,它们在水中电离出的离子如表所示:
如图1所示装置中,甲、乙、丙三个烧杯中依次盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极.接通电源,经过一段时间后,测得乙中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系如图2所示.请回答下列问题:
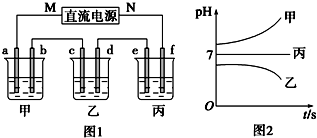
(1)M为直流电源的负极,b电极上发生的电极反应为4OH--4e-=2H2O+O2↑
(2)计算e电极上生成的气体在标准状况下的体积为5.6L
(3)写出乙烧杯中的总反应的离子方程式:2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2SO4
(4)要使丙烧杯中的C溶液恢复到原来的状态,需要进行的操作是:(写出要加入的物质和质量)向丙烧杯中加4.5 g水.
如图1所示装置中,甲、乙、丙三个烧杯中依次盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极.接通电源,经过一段时间后,测得乙中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系如图2所示.请回答下列问题:
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42-、OH- |

(1)M为直流电源的负极,b电极上发生的电极反应为4OH--4e-=2H2O+O2↑
(2)计算e电极上生成的气体在标准状况下的体积为5.6L
(3)写出乙烧杯中的总反应的离子方程式:2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2SO4
(4)要使丙烧杯中的C溶液恢复到原来的状态,需要进行的操作是:(写出要加入的物质和质量)向丙烧杯中加4.5 g水.
1.下列说法不正确的是( )
| A. | 已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 | |
| B. | 已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g),△H=+489.0 kJ/mol CO(g)+1/2O2(g)═CO2(g),△H=-283.0 kJ/mol C(石墨)+O2(g)═CO2(g),△H=-393.5 kJ/mol 则4Fe(s)+3O2(g)═2Fe2O3(s),△H=-1641.0 kJ/mol | |
| C. | 在0.1mol/L的氨水中加水稀释,氨水的导电能力降低 | |
| D. | 已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,Ka=$\frac{(ca)^{2}}{c(1-a)}$.若加入少量醋酸钠固体,则CH3COOH?CH3COO-+H+向左移动,α减小,Ka变小 |
11.下列各组中的两种物质,能用淀粉碘化钾试纸检验的是( )
| A. | 溴水和碘水 | B. | 盐酸和稀硫酸 | C. | 溴水和稀HCl | D. | 浓HNO3和氯水 |
18.由反应:2FeCl3+Cu→2FeCl2+CuCl2 推断出的氧化性或还原性强弱的结论,正确的是( )
| A. | 氧化性 Cu2+>Fe2+ | B. | 氧化性 Fe3+>Cu2+ | ||
| C. | 还原性 Fe2+>Cu | D. | 还原性 Fe>Cu |
16.将足量C02通入下列各溶液中,所含离子还能大量共存的是( )
| A. | K+、SiO32-、Cl-、NO3- | B. | Cu2+、NH4+、Al3+、SO42- | ||
| C. | Na+、S2-、OH-、SO42- | D. | Na+、ClO-、CH3COO-、HCO3- |