题目内容
11.有机物甲能发生银镜反应,甲催化加氢还原成有机物乙,1mol乙跟足量的金属钠反应放出标准状况下氢气22.4L,据此推断乙一定不是( )| A. | HOCH2CH2OH | B. | HOCH2CH(OH)CH3 | C. | CH3CH2CH2OH | D. | CH3CH(OH)CH(OH)CH3 |
分析 有机物甲能发生银镜反应,含有-CHO,为醛或甲酸形成的酯,甲催化加氢还原成有机物乙,则乙中含有羟基,1mol乙跟足量的金属钠反应放出标准状况下H222.4L,氢气的物质的量为1mol,说明乙中含有2个羟基或1个羟基、1个羧基,结合选项判断乙的可能结构,据此解答.
解答 解:A.甲为OHCCHO或HOCH2CHO,能发生银镜反应,能与氢气发生加成反应,生成乙为HOCH2CH2OH,1molHOCH2CH2OH与钠反应生成1mol氢气,故A正确;
B.若乙为HOCH2CH(OH)CH3,1mol乙与钠反应生成1mol氢气,甲与氢气发生加成反应生成乙,则甲可以为OHCCH(OH)CH3能发生银镜反应,故B正确;
C.若乙为CH3CH2OH,1mol乙与钠反应生成0.5mol氢气,故C错误;
D.若乙为CH3CH(OH)CH(OH)CH3,1mol乙与钠反应生成1mol氢气,甲与氢气发生加成反应生成乙,则甲不可能含有-CHO,甲不能发生银镜反应,故D错误.
故选CD.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析能力的考查,难度中等,掌握官能团的性质与转化是关键,注意利用验证法进行解答.

练习册系列答案
相关题目
8.某反应的化学方程式为:aFeCl2+bKNO3+cHCl═dFeCl3+eKCl+fX+gH2O,若b=1,d=3,则X的化学式为( )
| A. | N2 | B. | NO | C. | NO2 | D. | NH4Cl |
2.下面的排序不正确的是( )
| A. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| B. | 沸点:CH4>SiH4>GeH4>SnH4 | |
| C. | 熔点由高到低:Al>Mg>Na | |
| D. | 晶格能由大到小:NaF>NaCl>NaBr>NaI |
19.醇广泛存在于自然界中,是一类重要的有机化合物,请判断下列物质中不属于醇类的是( )
| A. | 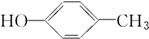 | B. | 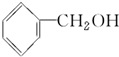 | C. | CH3OH | D. | 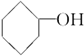 |
16.下表列出了A~R十二种元素在周期表中的位置:
请用相应的化学符号和化学用语回答下列问题:
(1)其中化学性质最不活泼的是Ar,最活泼的金属元素是K;
(2)A、C、D三种元素的氧化物对应的水化物,其中碱性最强的是NaOH;其中J与F按原子个数1:1所成的化合物的电子式为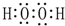 .
.
(3)A、B、C三种元素按离子半径由大到小的顺序排列为K+>Na+>Mg2+;
(4)E和J形成原子个数比为1:3化合物的结构简式CH3CH3,该物质与G的单质在一定条件下发生取代反应生成的二取代产物有2种.
(5)元素G的气态氢化物比元素H的气态氢化物稳定(填“稳定”或“不稳定”).元素K和I的气态氢化物沸点较高的是NH3(填化学式).其原因是氨气分子之间存在氢键.
(6)元素G的单质溶于元素A的最高价氧化物对应的水化物中,可生成具有漂白作用的一种盐,该盐的化学式为NaClO,该化合物中所含的化学键类型为_离子键、共价键.
(7)元素B、C、D的简单阳离子的氧化性比较Al3+>Mg2+>Na+.(填离子符号)
(8)1g元素J的单质完全燃烧生成液态氧化物时放出的热量为142.9KJ,写出元素J的单质燃烧热的热化学方程式:H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ•mol-1 .
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | J | |||||||
| 2 | E | K | F | |||||
| 3 | A | C | D | I | G | R | ||
| 4 | B | H |
(1)其中化学性质最不活泼的是Ar,最活泼的金属元素是K;
(2)A、C、D三种元素的氧化物对应的水化物,其中碱性最强的是NaOH;其中J与F按原子个数1:1所成的化合物的电子式为
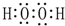 .
.(3)A、B、C三种元素按离子半径由大到小的顺序排列为K+>Na+>Mg2+;
(4)E和J形成原子个数比为1:3化合物的结构简式CH3CH3,该物质与G的单质在一定条件下发生取代反应生成的二取代产物有2种.
(5)元素G的气态氢化物比元素H的气态氢化物稳定(填“稳定”或“不稳定”).元素K和I的气态氢化物沸点较高的是NH3(填化学式).其原因是氨气分子之间存在氢键.
(6)元素G的单质溶于元素A的最高价氧化物对应的水化物中,可生成具有漂白作用的一种盐,该盐的化学式为NaClO,该化合物中所含的化学键类型为_离子键、共价键.
(7)元素B、C、D的简单阳离子的氧化性比较Al3+>Mg2+>Na+.(填离子符号)
(8)1g元素J的单质完全燃烧生成液态氧化物时放出的热量为142.9KJ,写出元素J的单质燃烧热的热化学方程式:H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ•mol-1 .
3.下列离子方程式书写正确的是( )
| A. | 向Fe2(SO4)3溶液中加入过量的Na2S:2Fe3++S2-=2Fe2++S↓ | |
| B. | 将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 用铜作电极电解饱和食盐水:2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 将铜屑加入Fe3+ 溶液中:2Fe3++Cu=2Fe2++Cu2+ |
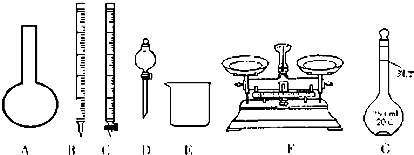
1.请选用适当的化学试剂和实验用品,用如图中的实验装置进行实验,证明过氧化钠可作供氧剂.
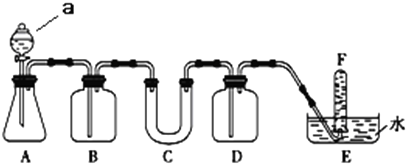
(1)A是制取CO2的装置.仪器a的名称分液漏斗写出A中发生反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)填写表中空格:(请在答题卡上填写)
(3)写出过氧化钠与二氧化碳反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.该反应中氧化剂与还原剂的物质的量之比为1:1
(4)如果实验室将1.5mol过氧化钠与3mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是Na2CO3.

(1)A是制取CO2的装置.仪器a的名称分液漏斗写出A中发生反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)填写表中空格:(请在答题卡上填写)
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| C | Na2O2 | 与CO2及水蒸气反应,产生O2 |
| D | . |
(4)如果实验室将1.5mol过氧化钠与3mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是Na2CO3.
 实验室制备乙酸乙酯,回答有关问题:
实验室制备乙酸乙酯,回答有关问题: CH3COOC2H5+H2O.
CH3COOC2H5+H2O.