题目内容
6. 实验室制备乙酸乙酯,回答有关问题:
实验室制备乙酸乙酯,回答有关问题:(1)写出在A中发生的化学方程式CH3COOH+CH3CH2OH
 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.(2)B中盛放的试剂是饱和碳酸钠溶液.
(3)反应中浓硫酸的作用是催化作用、吸水作用.
(4)反应后得到乙酸乙酯的操作方法是分液.
分析 (1)酯化反应的本质为酸脱羟基,醇脱氢,在A中反应生成乙酸乙酯和水,且为可逆反应;
(2)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,目的是除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层;
(3)乙酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;
(4)分离互不相溶的液体通常用分液的方法.
解答 解:(1)酯化反应的本质为酸脱羟基,醇脱氢,在A中乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应方程式为:CH3COOH+CH3CH2OH CH3COOC2H5+H2O,
CH3COOC2H5+H2O,
故答案为:CH3COOH+CH3CH2OH CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
(2)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层,所以b中盛放的液体为饱和碳酸钠溶液,
故答案为:饱和碳酸钠溶液;
(3)乙酸与乙醇发生酯化反应,该反应为可逆反应,需浓硫酸作催化剂,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,故浓硫酸的作用为催化剂、吸水剂,
故答案为:催化作用、吸水作用;
(4)因B中的液体混合物分层不互溶,乙酸乙酯在上层,可用分液方法分离,
故答案为:分液.
点评 本题考查乙酸乙酯的制备,题目难度不大,注意理解饱和碳酸钠溶液的作用以及酯化反应的机理,试题培养了学生分析、理解能力及灵活应用所学知识解决实际问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.某校老师和学生用相同质量和相同形状的锌片和不同浓度的足量稀盐酸反应得到实验数据如表所示:
Ⅰ.实验①和②探究的是:(1)温度对反应速率的影响
该反应的离子方程式为:(2)Zn+2H+=Zn2++H2↑.
Ⅱ.实验②和③表明:(3)盐酸浓度越大,化学反应速率越大;
Ⅲ.除上述条件的改变引起速率的改变外,还可能有那些因素加快上述反应速率:
(4)锌的颗粒大小(列举其中一个因素)
Ⅳ.如果把实验③中锌片换成相同质量的铁片,请比较两种金属中那种产生的氢气多并说明原因:
(5)铁产生的氢气多,铁的摩尔质量小于锌,相同质量的铁锌,铁的物质的量多,失电子多(每摩尔铁锌均失2mole-).
| 实验编号 | 盐酸浓度 | 反应温度/℃ | 收集100mL氢气所需时间/s |
| ① | 1mol/L | 15 | 200 |
| ② | 1mol/L | 25 | 90 |
| ③ | 2mol/L | 25 | 10 |
该反应的离子方程式为:(2)Zn+2H+=Zn2++H2↑.
Ⅱ.实验②和③表明:(3)盐酸浓度越大,化学反应速率越大;
Ⅲ.除上述条件的改变引起速率的改变外,还可能有那些因素加快上述反应速率:
(4)锌的颗粒大小(列举其中一个因素)
Ⅳ.如果把实验③中锌片换成相同质量的铁片,请比较两种金属中那种产生的氢气多并说明原因:
(5)铁产生的氢气多,铁的摩尔质量小于锌,相同质量的铁锌,铁的物质的量多,失电子多(每摩尔铁锌均失2mole-).
17.可逆反应:2NO(g)+O2(g)═2NO2(g),在体积不变的密闭容器中反应,一定达到平衡状态的标志是( )
| A. | 单位时间内生成n mol O2的同时生成n mol NO2 | |
| B. | 混合气体的颜色不再改变的状态 | |
| C. | ν(NO2):ν(NO):ν(O2)=2:2:1的状态 | |
| D. | 混合气体的密度不再改变的状态 |
14.某无色透明的强酸性溶液中,能大量共存的一组离子是( )
| A. | Al3+、SO42-、Cl- | B. | Na+、AlO2- K+、SO42- | ||
| C. | MnO${\;}_{4}^{-}$、K+、SO42-、Na+ | D. | NH4+、NO3-、Fe2+、Cl- |
11.有机物甲能发生银镜反应,甲催化加氢还原成有机物乙,1mol乙跟足量的金属钠反应放出标准状况下氢气22.4L,据此推断乙一定不是( )
| A. | HOCH2CH2OH | B. | HOCH2CH(OH)CH3 | C. | CH3CH2CH2OH | D. | CH3CH(OH)CH(OH)CH3 |
15.聚乙炔导电聚合物的合成使高分子材料进入了“合成金属”和塑料电子学时代.以下是我国化学家近年来合成的聚乙炔衍生物分子M的结构式及M在稀硫酸作用下的水解过程示意图;下列有关说法中错误的是( )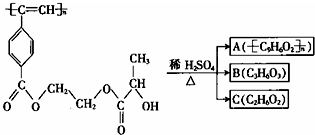

| A. | M和A均能使酸性KMnO4溶液和溴水褪色 | |
| B. | B(C3H6O3)能发生消去反应和酯化反应 | |
| C. | 1mol M与足量热的烧碱溶液反应,最多可消耗2n mol NaOH | |
| D. | A、B、C各1mol分别与足量金属钠反应,放出气体的物质的量之比为1:2:2 |
16.下列说法中,正确的是( )
| A. | 石油常压分馏可得直馏汽油,石油汽可用作石油裂化的原料 | |
| B. | 石油裂解的目的是为了得到乙烯、丙烯和甲烷等化工原料 | |
| C. | 煤的干馏发生了物理变化,石油的减压分馏是化学变化 | |
| D. | 煤中含有苯和甲苯,可以通过先干馏后分馏的方法得到苯和甲苯 |

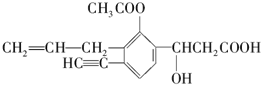 某有机化合物结构如下,分析其结构并完成下列问题:
某有机化合物结构如下,分析其结构并完成下列问题: