题目内容
【题目】A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处在同一周期,A、C处在同一主族。C原子核内质子数等于A、B原子核内质子数之和,C原子最外层上的电子数是D原子最外层电子数的4倍。试回答:
(1)这四种元素名称分别是:A___________,B___________,C___________,D___________。
(2)这四种元素中在常温常压下的液态或气态氢化物的稳定性由大而小的顺序是_______________。(用化学式表示,下同)
(3)A与B形成的三原子分子的电子式是___________,B与D形成的原子个数比为l∶l的化合物中含有的化学键类型有___________。
(4)写一个能证明A和C的金属性或者非金属性强弱的化学方程式是___________。
【答案】(1)碳氧硅钠
(2)H2O>CH4>SiH4
(3)![]() 离子键和共价键
离子键和共价键
(4) Na2SiO3+ CO2+ H2O= Na2CO3+ H2SiO3↓
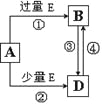
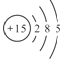
【解析】试题分析:A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处在同一周期,A、C处在同一主族,四种元素在周期表中的大致相对位置为![]() ,A、C处在同一主族,二者质子数相差8,C原子核内质子数等于A、B原子核内质子数之和,B的质子数为8,B为O元素;C原子最外层上的电子数是D原子最外层电子数的4倍,C最外层电子数为4,D的最外层电子数为1,A为C元素,C为Si元素,D为Na元素,据此解答该题。
,A、C处在同一主族,二者质子数相差8,C原子核内质子数等于A、B原子核内质子数之和,B的质子数为8,B为O元素;C原子最外层上的电子数是D原子最外层电子数的4倍,C最外层电子数为4,D的最外层电子数为1,A为C元素,C为Si元素,D为Na元素,据此解答该题。
(1)根据上述推断,A、B、C、D元素的名称分别为碳、氧、硅、钠。
(2)四种元素中在常温常压下有液态或气态氢化物的为C、O、Si,它们的非金属性O>C>Si,氢化物的稳定性为H2O>CH4>SiH4。
(3)A与B形成的三原子分子为CO2,其电子式是![]() ,B与D形成的原子个数比为1:1的化合物为过氧化钠,含有的化学键类型有离子键和共价键。
,B与D形成的原子个数比为1:1的化合物为过氧化钠,含有的化学键类型有离子键和共价键。
(4)根据上述推断,A和C分别为C、Si,非金属性越强,最高价含氧酸的酸性越强,若碳酸能和硅酸钠反应生成碳酸钠和硅酸(白色沉淀),则非金属性C>Si,化学方程式为Na2SiO3+ CO2+ H2O= Na2CO3+ H2SiO3↓。