题目内容
3.下列离子组在一定条件下能大量共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是( )| 选项 | 离子组 | 加入试剂(溶液) | 加入试剂后发生反应的离子方程式 |
| A | SO42-、Fe2+、NO3-、K+ | K3[Fe(CN)6] | 3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓ |
| B | Na+、Fe3+、I-、ClO- | HCl | ClO-+H+=HClO |
| C | Ba2+、Al3+、Cl-、H+ | 少量NaOH | Al3++3OH-=Al(OH)3↓ |
| D | S2O32-、Na+、Cl-、SO32-、K+ | 过量硫酸 | 2S2O32-+2H+=SO42-+3S↓+H2O |
| A. | A | B. | B | C. | C | D. | D |
分析 A.加入K3[Fe(CN)6]后,Fe2+可与[Fe(CN)6]2-反应;
B.Fe3+、I-、ClO-发生氧化还原反应;
C.氢离子结合氢氧根离子能力大于铝离子,氢氧化钠少量,氢离子优先反应;
D.加过量硫酸后S2O32-和亚硫酸根离子都与氢离子反应.
解答 解:A.SO42-、Fe2+、NO3-、K+离子之间不发生反应,Fe2+可与[Fe(CN)6]2-反应,反应的离子方程式为:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,故A正确;
B.I-与Fe3+、ClO-发生氧化还原反应,在溶液中不能大量共存,故B错误;
C.加入少量的NaOH,H+优先与NaOH反应,正确的离子方程式为:OH-+H+=H2O,故C错误;
D.该组离子之间不反应,可大量共存,但加过量硫酸后S2O32-和SO32-都与氢离子反应,反应的离子反应为:S2O32-+2H+=SO2+S↓+H2O、SO32-+2H+=SO2↑+H2O,故D错误;
故选A.
点评 本题考查了离子共存、离子方程式的书写判断,题目难度中等,明确离子反应发生条件及离子方程式的书写原则为解答关键,注意题干要求“离子组在一定条件下能大量共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确”.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
5.可用一种试剂鉴别KCl、Ba(OH)2、Na2CO3、K2SO3四种溶液,该试剂是( )
| A. | BaCl2 | B. | H2SO4 | C. | KOH | D. | HCl |
6.下列物质之间的转化,能一步完成的是( )
| A. | CH3CH2OH→CH3CHO | B. | Fe2O3→Fe(OH)3 | C. | SiO2→H2SiO3 | D. | Al2O3→Al(OH)3 |
11.将Mg、Cu组成的2.64g混合物投入适量稀硝酸中恰好完全反应,固体完全溶解时收集到还原产物NO气体0.896L(标准状况),向反应后的溶液中加入一定体积1mol•L-1的NaOH溶液恰好使金属离子沉淀完全,则加入NaOH溶液的体积为( )
| A. | 80ml | B. | 120ml | C. | 150ml | D. | 200ml |
8.以下说法错误的是( )
| A. | 银氨溶液可用于区分麦芽糖和葡萄糖 | |
| B. | 乙烷、乙醛、乙酸的沸点逐渐升高 | |
| C. | 1mol乙酰水杨酸(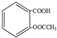 )最多可以和3molNaOH反应 )最多可以和3molNaOH反应 | |
| D. | 邻甲基苯酚(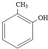 )可以和HCHO发生缩聚反应 )可以和HCHO发生缩聚反应 |
15.下表是A、B两种有机物的有关信息:
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称是1,2-二溴乙烷.
(2)A与氢气发生加成反应后生成分子C,C在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体②有毒③不溶于水④密度比水大⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应;在浓硫酸作用下,B与浓硝酸反应的化学方程式是 .
.
| A | B |
| ①由C、H两种元素组成; ②能使溴的四氯化碳溶液褪色; ③比例模型为:  | ①由C、H两种元素组成; ②球棍模型为:  |
(1)A与溴的四氯化碳溶液反应的生成物的名称是1,2-二溴乙烷.
(2)A与氢气发生加成反应后生成分子C,C在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体②有毒③不溶于水④密度比水大⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应;在浓硫酸作用下,B与浓硝酸反应的化学方程式是
 .
.
13.根据总反应式:Zn+Cu2+=Zn2++Cu,请分析下述原电池的组成,对应正确的一组是( )
| A | B | C | D | |
| 正极 | Cu | Cu | Zn | Ag |
| 负极 | Zn | Zn | Cu | Cu |
| 电解质溶液 | CuSO4 | AgNO3 | CuCl2 | CuSO4 |
| A. | A | B. | B | C. | C | D. | D |


 ;
; ,在核磁共振氢谱中出现5组峰.
,在核磁共振氢谱中出现5组峰.