题目内容
5.可用一种试剂鉴别KCl、Ba(OH)2、Na2CO3、K2SO3四种溶液,该试剂是( )| A. | BaCl2 | B. | H2SO4 | C. | KOH | D. | HCl |
分析 只用一种试剂鉴别KCl、Ba(OH)2、Na2CO3、K2SO3四种溶液,反应的现象应各不相同,稀H2SO4与K2SO3反应生成刺激性气味的气体,稀H2SO4与BaCl2反应生成白色沉淀,稀H2SO4与Na2CO3反应生成气体,与KCl不反应以此来解答.
解答 解:A、BaCl2与KCl、Ba(OH)2不发生反应,与Na2CO3、K2SO3都生成白色沉淀,不能鉴别,故A错误;
B、稀H2SO4与K2SO3反应生成刺激性气味的气体,稀H2SO4与BaCl2反应生成白色沉淀,稀H2SO4与Na2CO3反应生成气体,与KCl不反应,可以一次鉴别四种物质,故B正确;
C、KOH与KCl、Ba(OH)2、Na2CO3、K2SO3 都不反应,不能鉴别,故C错误;
D、HCl与KCl不发生反应,与Ba(OH)2 反应但无现象,Na2CO3 、K2SO3反应分别反应生成无色无味气体二氧化碳和无色刺激性气味的气体二氧化硫,不能一次鉴别,故D错误;
故选B.
点评 本题考查物质的鉴别,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握物质的性质的异同,鉴别物质时应具有明显的不同现象,难度不大.

练习册系列答案
相关题目
16.把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池.A、B相连时,A为负极;C、D相连时,D上有气泡逸出;A、C相连时,A极减轻;B、D相连时,B为正极.则四种金属的活动性顺序由大到小排列为( )
| A. | A>B>C>D | B. | A>C>B>D | C. | A>C>D>B | D. | B>D>C>A |
17.下列有说法不正确的是( )
| A. | 离子晶体的晶格能是气态离子形成1mol晶胞时放出的能量 | |
| B. | 金属的六方最密堆积和面心立方最密堆积的空间利用率最高 | |
| C. | 钠晶胞结构如图 ,钠晶胞中每个钠原子的配位数为8 ,钠晶胞中每个钠原子的配位数为8 | |
| D. | 温度升高,金属的导电性将变弱 |
14. 甲--辛等元素在周期表中的相对位置如图.甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素,下列判断正确的是( )
甲--辛等元素在周期表中的相对位置如图.甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素,下列判断正确的是( )
 甲--辛等元素在周期表中的相对位置如图.甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素,下列判断正确的是( )
甲--辛等元素在周期表中的相对位置如图.甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素,下列判断正确的是( )| A. | 金属性:甲>乙>丁 | |
| B. | 原子半径:辛>己>戊 | |
| C. | 丙与庚的原子核外电子数相差14 | |
| D. | 乙的单质在空气中燃烧生成只含离子键的化合物 |
3.下列离子组在一定条件下能大量共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是( )
| 选项 | 离子组 | 加入试剂(溶液) | 加入试剂后发生反应的离子方程式 |
| A | SO42-、Fe2+、NO3-、K+ | K3[Fe(CN)6] | 3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓ |
| B | Na+、Fe3+、I-、ClO- | HCl | ClO-+H+=HClO |
| C | Ba2+、Al3+、Cl-、H+ | 少量NaOH | Al3++3OH-=Al(OH)3↓ |
| D | S2O32-、Na+、Cl-、SO32-、K+ | 过量硫酸 | 2S2O32-+2H+=SO42-+3S↓+H2O |
| A. | A | B. | B | C. | C | D. | D |
 已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.
已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.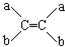 和
和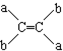 两种结构式互为同分异构体(a、b为不同的原子或原子团),被称为烯烃的顺反异构,试推断一氯丙烯的同分异构体(不含环状结构)共有( )
两种结构式互为同分异构体(a、b为不同的原子或原子团),被称为烯烃的顺反异构,试推断一氯丙烯的同分异构体(不含环状结构)共有( )