题目内容
11.将Mg、Cu组成的2.64g混合物投入适量稀硝酸中恰好完全反应,固体完全溶解时收集到还原产物NO气体0.896L(标准状况),向反应后的溶液中加入一定体积1mol•L-1的NaOH溶液恰好使金属离子沉淀完全,则加入NaOH溶液的体积为( )| A. | 80ml | B. | 120ml | C. | 150ml | D. | 200ml |
分析 Mg、Cu混合物与硝酸恰好反应生成Mg(NO3)2、Cu(NO3)2,部分硝酸被还原为NO气体,标况下0.896LNO气体的物质的量为:$\frac{0.896L}{22.4L/mol}$=0.04mol,根据电子守恒,Mg、Cu失去电子的物质的量为:0.04mol(5-2)=0.12mol,则反应后生成镁离子、铜离子的总物质的量为:$\frac{0.12mol}{2}$=0.06mol;向反应后的溶液中加入一定体积1mol•L-1的NaOH溶液恰好使金属离子沉淀完全,则氢氧化钠提供的氢氧根离子所带电荷与镁离子、铜离子所带电荷相等,据此可知氢氧化钠物质的量,再根据V=$\frac{n}{c}$计算出消耗氢氧化钠溶液的体积.
解答 解:Mg、Cu混合物与硝酸恰好反应生成Mg(NO3)2、Cu(NO3)2,部分硝酸被还原为NO气体,
标况下0.896LNO气体的物质的量为:$\frac{0.896L}{22.4L/mol}$=0.04mol,根据电子守恒,Mg、Cu失去电子的物质的量为:0.04mol(5-2)=0.12mol,则反应后生成镁离子、铜离子的总物质的量为:$\frac{0.12mol}{2}$=0.06mol,
向反应后的溶液中加入一定体积1mol•L-1的NaOH溶液恰好使金属离子沉淀完全,则氢氧化钠提供的氢氧根离子所带电荷与镁离子、铜离子所带电荷相等,则氢氧化钠的物质的量为:0.06mol×2=0.12mol,
消耗1mol•L-1的NaOH溶液的体积为:$\frac{0.12mol}{1mol/L}$=0.12L=120mL,
故选B.
点评 本题考查混合物反应的计算,题目难度中等,判断金属提供电子等于氢氧根的物质的量是解题关键,注意守恒思想在化学计算中的应用方法.

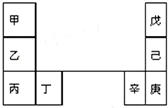 甲--辛等元素在周期表中的相对位置如图.甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素,下列判断正确的是( )
甲--辛等元素在周期表中的相对位置如图.甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素,下列判断正确的是( )| A. | 金属性:甲>乙>丁 | |
| B. | 原子半径:辛>己>戊 | |
| C. | 丙与庚的原子核外电子数相差14 | |
| D. | 乙的单质在空气中燃烧生成只含离子键的化合物 |
| A. | 当c(Cu2+)=c(Mn2+)时该反应达到平衡 | |
| B. | 从该反应原理可以得出CuS的溶解度比MnS的溶解度大 | |
| C. | 该反应的平衡常数K=$\frac{{K}_{sp}(MnS)}{{K}_{sp}(CuS)}$ | |
| D. | 往平衡体系中加入少量CuSO4(s)后,c( Mn2+)不变 |
(1)已知:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ/mol,达到平衡后,体积不变时,能提高H2O的平衡转化率的措施是AD.
A.升高温度B.增加碳的用量C.加入催化剂D.用储氢金属吸收H2

(2)某些合金可用于储存氢,金属储氢的原理可表示为:M(s)+xH2(g)?MH2(s)△H<0(M表示某种合金).如图1表示温度分别为T1、T2时,最大吸氢量与氢气压强的关系,则T1<T2(填“<”、“>”或“=”).
(3)某温度下,在2L体积不变的密闭容器中将1molCO和2molH2混合发生反应:CO(g)+2H2(g)?CH3OH(g),测得不同时刻的反应前后压强关系如表:
| 时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强比($\frac{{P}_{后}}{{P}_{前}}$) | 0.98 | 0.90 | 0.78 | 0.66 | 0.66 | 0.66 |
(4)CO可以还原某些金属氧化物生成金属单质和CO2,如图2是四种金属氧化物被CO还原时1g[$\frac{c(CO)}{c(C{O}_{2})}$)]与温度(T)的关系曲线图.
①其中最易被还原的金属氧化物是Cu2O(填化学式).
②700℃时CO还原Cr2O3反应中的平衡常数k=10-12.
(5)水煤气处理后,获得的较纯H2用于合成氨:N2(g)+3H2(g)?2NH3(g),△H=-92.4kJ•mol-1.如图3为不同实验条件下进行合成氨反应实验,N2浓度随时间变化示意图.
①与实验Ⅰ比较,实验Ⅱ改变的条件为使用催化剂.
②实验Ⅲ比实验Ⅰ的温度要高,其它条件相同,请在图4中画出实验Ⅰ和实验Ⅲ中NH3浓度随时间变化的示意图
 .
.(6)饮用水中的NO3-主要来自于NH4+,已知在微生物作用下,NH4+经过两步反应被氧化成NO3-,两步反应的能量变化示意图如图5.请写出1molNH4+(aq)的热化学方程式NH4+(aq)+2O2(g)═2H+(aq)+H2O(l)+NO3-(aq),△H=-346 kJ/mol.

| A. | -OH | B. | -C≡C- | C. |  | D. | C-C |
| 选项 | 离子组 | 加入试剂(溶液) | 加入试剂后发生反应的离子方程式 |
| A | SO42-、Fe2+、NO3-、K+ | K3[Fe(CN)6] | 3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓ |
| B | Na+、Fe3+、I-、ClO- | HCl | ClO-+H+=HClO |
| C | Ba2+、Al3+、Cl-、H+ | 少量NaOH | Al3++3OH-=Al(OH)3↓ |
| D | S2O32-、Na+、Cl-、SO32-、K+ | 过量硫酸 | 2S2O32-+2H+=SO42-+3S↓+H2O |
| A. | A | B. | B | C. | C | D. | D |
| A. | C、D、E、A、B | B. | E、C、D、A、B | C. | B、A、D、C、E | D. | B、A、E、D、C |
| A. | 强酸性溶液中:NH4+、K+、CO32-、Cl- | |
| B. | 有SO42-存在的溶液中:Na+、Mg2+、Ba2+、I- | |
| C. | 加入铝粉能放出氢气的溶液中:K+、Ba2+、Cl-、Br- | |
| D. | 在强碱性的溶液中:NH4+、Na+、Cl-、H+ |
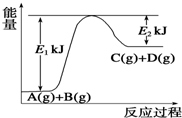 已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.
已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.