题目内容
18.常温下,下列各组离子一定能在指定溶液中大量共存的是( )| A. | 使酚酞变红色的溶液中:Na+、Al3+、SO42-、Cl- | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| C. | 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42- | |
| D. | 水电离的c(H+)=1×10-13mol•L-1的溶液中:K+、Na+、AlO2-、CO32- |
分析 A.使酚酞变红色的溶液,显碱性;
B.$\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液,显酸性;
C.与Al反应能放出H2的溶液,为非氧化性酸或强碱溶液;
D.水电离的c(H+)=1×10-13mol•L-1的溶液,水的电离受到抑制,为酸或碱溶液.
解答 解:A.使酚酞变红色的溶液,显碱性,碱性溶液中不能大量存在Al3+,故A错误;
B.$\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液,显酸性,该组离子在酸性溶液中不反应,可大量共存,故B正确;
C.与Al反应能放出H2的溶液,为非氧化性酸或强碱溶液,酸性溶液中Fe2+(或Al)、H+、NO3-发生氧化还原反应,碱性溶液中不能大量存在Fe2+,故C错误;
D.水电离的c(H+)=1×10-13mol•L-1的溶液,水的电离受到抑制,为酸或碱溶液,酸溶液中不能大量存在AlO2-、CO32-,故D错误;
故选B.
点评 本题考查离子的共存,为2015年高考题,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,注意“一定共存”的信息,题目难度不大.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
8.下列区分苯和己烯的试验方法和判断正确的是( )
| A. | 分别点燃,无黑烟生成的是苯 | |
| B. | 分别加入溴水振荡,静置后分层,橙黄色消失的是己烯 | |
| C. | 分别加入溴的CCl4,静置后分层,上下两层均为无色的是已烯 | |
| D. | 分别加入酸性KMnO4溶液振荡,紫色消失的是己烯 |
9.10mL浓度为1mol•L-1的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成量的是( )
| A. | K2SO4 | B. | CH3COONa | C. | CuSO4 | D. | Na2CO3 |
6.下列说法不正确的是( )
| A. | Na与H2O的反应是熵增的放热反应,该反应能自发进行 | |
| B. | 饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同 | |
| C. | FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 | |
| D. | Mg(OH)2固体在溶液存在平衡:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 |
13.“保护环境”是我国的基本国策.下列做法不应该提倡的是( )
| A. | 采取低碳、节俭的生活方式 | |
| B. | 按照规定对生活废弃物进行分类放置 | |
| C. | 深入农村和社区宣传环保知识 | |
| D. | 经常使用一次性筷子、纸杯、塑料袋等 |
3.下列说法正确的是( )
| A. | 若H2O2分解产生1molO2,理论上转移的电子数约为4×6.02×1023 | |
| B. | 室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,溶液pH>7 | |
| C. | 钢铁水闸可用牺牲阳极或外加电流的阴极保护法防止其腐蚀 | |
| D. | 一定条件下反应N2+3H2?2NH3达到平衡时,3v正(H2)=2v逆(NH3) |
18.已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,下列说法正确的是( )
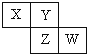

| A. | Z单质的化学活泼性一定比Y单质的强 | |
| B. | W的原子序数可能是Y的原子序数的2倍 | |
| C. | W的气态氢化物的稳定性一定比Y的强 | |
| D. | X和W两元素不可能形成共价化合物 |
19.化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A. | 通过红外光谱分析可以区分乙醇与乙酸乙酯 | |
| B. | 煎炸食物的花生油和牛油都是可皂化的饱和酯类 | |
| C. | 淀粉可用于制备葡萄糖、酿制食醋,还可作药片的赋形剂 | |
| D. | 利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学方法 |