��Ŀ����
��Ӧ2CH3OH��l��+3O2��g���T2CO2��g��+4H2O��l�������е������仯��ͼ1��ʾ��
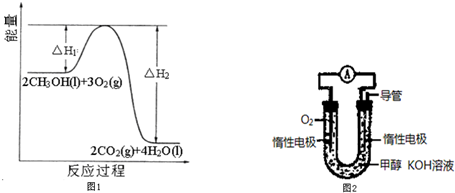
��ע����H1=+a kJ/mol����H2=-b kJ/mol��a��b������0��
�ش��������⣺
��1���÷�Ӧ�� ��Ӧ������ȡ������ȡ���
��2����Ӧ��ϵ�м�������Է�Ӧ���Ƿ���Ӱ�죿 ����С�����û�С�����
��3���÷�Ӧ���淴Ӧ�Ļ��Ϊ ��
��4��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ���������ͼ2��ʾ��ԭ���װ�ã��õ�ظ����缫��ӦʽΪ ��
��5���״�ȼ�ղ���CO2����Ȼ��ѭ��ʱҲ����CaCO3��Ӧ��CaCO3��һ���������ʣ���Ksp=2.8��10-9����0.6mol/L��CaCl2��Һ��2.0mol/L��Na2CO3��Һ�������ϣ����Ϻ�����ӵ�Ũ��Ϊ ��

��ע����H1=+a kJ/mol����H2=-b kJ/mol��a��b������0��
�ش��������⣺
��1���÷�Ӧ��
��2����Ӧ��ϵ�м�������Է�Ӧ���Ƿ���Ӱ�죿
��3���÷�Ӧ���淴Ӧ�Ļ��Ϊ
��4��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ���������ͼ2��ʾ��ԭ���װ�ã��õ�ظ����缫��ӦʽΪ
��5���״�ȼ�ղ���CO2����Ȼ��ѭ��ʱҲ����CaCO3��Ӧ��CaCO3��һ���������ʣ���Ksp=2.8��10-9����0.6mol/L��CaCl2��Һ��2.0mol/L��Na2CO3��Һ�������ϣ����Ϻ�����ӵ�Ũ��Ϊ
���㣺��Ӧ�Ⱥ��ʱ�
ר�⣺��ѧ��Ӧ�е������仯
��������1��ͼ���������Ӧ�����������������Ӧ���ȣ�
��2�������ı䷴Ӧ���ʣ����ı仯ѧƽ�⣬���ı䷴Ӧ�ķ�Ӧ�ȣ�
��3��ͼ������淴Ӧ�Ļ����ָ���������������Ҫ�����������Ϊ��ֵ��
��4���״�ȼ�ϵ����ȼ�ϼ״��ڸ���ʧ���ӷ���������Ӧ������Һ������̼���Σ���ϵ���غ���д�缫��Ӧ��
��5�������ܶȻ��������������Ũ�ȼ��㣮
��2�������ı䷴Ӧ���ʣ����ı仯ѧƽ�⣬���ı䷴Ӧ�ķ�Ӧ�ȣ�
��3��ͼ������淴Ӧ�Ļ����ָ���������������Ҫ�����������Ϊ��ֵ��
��4���״�ȼ�ϵ����ȼ�ϼ״��ڸ���ʧ���ӷ���������Ӧ������Һ������̼���Σ���ϵ���غ���д�缫��Ӧ��
��5�������ܶȻ��������������Ũ�ȼ��㣮
���
�⣺��1��ͼ���������Ӧ����������������������2CH3OH��l��+3O2��g���T2CO2��g��+4H2O��l������H=-��b-a��KJ/mol��Ӧ�Ƿ��ȷ�Ӧ��
�ʴ�Ϊ�����ȣ�
��2�������ı䷴Ӧ���ʣ����ı仯ѧƽ�⣬��Ӧ��ϵ�м�������Է�Ӧ����Ӱ�죻
�ʴ�Ϊ��û�У�
��3���淴Ӧ�Ļ����ָ���������������Ҫ���������÷�Ӧ���淴Ӧ�Ļ��Ϊb KJ?mo1-1��-��H2��
�ʴ�Ϊ��b KJ?mo1-1��-��H2��
��4���״�ȼ�ϵ����ȼ�ϼ״��ڸ���ʧ���ӷ���������Ӧ������Һ������̼���Σ������缫��ӦΪ��CH3OH-6e-+8OH-=CO32-+6H2O��
�ʴ�Ϊ��CH3OH-6e-+8OH-=CO32-+6H2O��
��5����0.6mol/L��CaCl2��Һ��2.0mol/L��Na2CO3��Һ�������ϣ�������ӦCa2++CO32-=CaCO3����ʣ��̼�������Ũ��Ϊ0.7mol/L�������ܶȻ�����Ksp=c��Ca2+��c��CO32-��=2.8��10-9��c��Ca2+��=
=4.0��10-9mol/L��
�ʴ�Ϊ��4.0��10-9mol/L��
�ʴ�Ϊ�����ȣ�
��2�������ı䷴Ӧ���ʣ����ı仯ѧƽ�⣬��Ӧ��ϵ�м�������Է�Ӧ����Ӱ�죻
�ʴ�Ϊ��û�У�
��3���淴Ӧ�Ļ����ָ���������������Ҫ���������÷�Ӧ���淴Ӧ�Ļ��Ϊb KJ?mo1-1��-��H2��
�ʴ�Ϊ��b KJ?mo1-1��-��H2��
��4���״�ȼ�ϵ����ȼ�ϼ״��ڸ���ʧ���ӷ���������Ӧ������Һ������̼���Σ������缫��ӦΪ��CH3OH-6e-+8OH-=CO32-+6H2O��
�ʴ�Ϊ��CH3OH-6e-+8OH-=CO32-+6H2O��
��5����0.6mol/L��CaCl2��Һ��2.0mol/L��Na2CO3��Һ�������ϣ�������ӦCa2++CO32-=CaCO3����ʣ��̼�������Ũ��Ϊ0.7mol/L�������ܶȻ�����Ksp=c��Ca2+��c��CO32-��=2.8��10-9��c��Ca2+��=
| 2.8��10-9 |
| 0.7 |
�ʴ�Ϊ��4.0��10-9mol/L��
���������⿼�����Ȼ�ѧ����ʽͼ�������ԭ���ԭ����Ӧ�úն��缫��Ӧ��д�������ܽ�ƽ����ܶȻ�����Ӧ�ã����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�
�����Ŀ
����˵����ȷ���ǣ�������
| A�������ᷴӦ�����κ�ˮ��������һ���Ǽ��������� |
| B����SO2ͨ����ˮ�У���ˮ������ɫ����������SO2����Ư������ |
| C����Ba��OH��2��Һ�ε�������Һ�У���SO42-ǡ�ó�����ȫʱ����ֻ��AlO2-��ʽ���� |
| D���ں���Cu��NO3��2��Mg��NO3��2��Fe��NO3��3��Һ�м������п�ۣ����ȱ���ԭ����Cu2+ |
�����йط�Ӧ�ȵ�������ȷ���ǣ�������
| A���������ѧ��Ӧ��һ�������¶���һ������ |
| B���������оݣ�NH4HCO3���ȷֽ���Է����� |
| C��ʹ�ô������ɽ��ͷ�Ӧ�Ļ�ܣ��ӿ췴Ӧ���ʣ��ı䷴Ӧ�� |
| D��FeCl3��KSCN��Ӧ�ﵽƽ��ʱ�������еμ�KCl��Һ������Һ��ɫ���� |
Ԫ�����ڱ���Ԫ�������ɿ���ָ�����ǽ��й����Ե��Ʋ���жϣ�����˵�����������ǣ�������
| A����ˮ��Һ�����ԣ�HCl��H2S�����ƶϳ�Ԫ�صķǽ����ԣ�Cl��S |
| B����X+��Y2-�ĺ�����Ӳ�ṹ��ͬ����ԭ��������X��Y |
| C����Ԫ�����ڱ��У��衢�λ�ڽ�����ǽ����Ľ��紦�����������뵼����� |
| D��Cs��Ba�ֱ�λ�ڵ������ڢ�A��͢�A�壬���ԣ�CsOH��Ba��OH��2 |
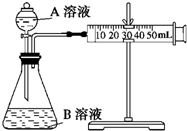 �ס�������ʵ��С������KMnO4������Һ��H2C2O4��Һ��Ӧ�о�Ӱ�췴Ӧ���ʵ����أ�
�ס�������ʵ��С������KMnO4������Һ��H2C2O4��Һ��Ӧ�о�Ӱ�췴Ӧ���ʵ����أ�