题目内容
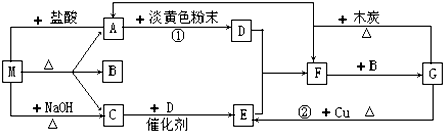
如图中的每1方格表示一种有关的反应物或生成物.其中A、C为无色气体.
完成下列问题:
(1)物质M可以是 ,F是 .
(2)反应①除生成D外,生成的另一种物质的水溶液显碱性,用离子方程式解释溶液显碱性的原因: .
(3)检验M中阳离子的方法: .
(4)G到E的离子反应方程式: ,每生成标况下1.12L的E,转移电子 mol.

完成下列问题:
(1)物质M可以是
(2)反应①除生成D外,生成的另一种物质的水溶液显碱性,用离子方程式解释溶液显碱性的原因:
(3)检验M中阳离子的方法:
(4)G到E的离子反应方程式:
考点:无机物的推断
专题:推断题
分析:M既能与盐酸反应,又能与NaOH反应,都生成气体,应为弱酸铵盐,则C为NH3,气体A能与淡黄色粉末反应,应是二氧化碳与过氧化钠反应,故A为CO2,则A应为碳酸铵或碳酸氢铵,B为H2O,结合转化关系可知,D为O2,E为NO,F为NO2,G为HNO3,结合物质的性质进行解答.
解答:
解:M既能与盐酸反应,又能与NaOH反应,都生成气体,应为弱酸铵盐,则C为NH3,气体A能与淡黄色粉末反应,应是二氧化碳与过氧化钠反应,故A为CO2,则A应为碳酸铵或碳酸氢铵,B为H2O,结合转化关系可知,D为O2,E为NO,F为NO2,G为HNO3,
(1)由上述分析可知,M为(NH4)2CO3 或NH4HCO3,F为NO2,
故答案为:NH4HCO3(或(NH4)2CO3);NO2;
(2)反应①除生成氧气外,生成的另一种物质为碳酸钠,碳酸钠为强碱弱酸盐,水解呈碱性,离子方程式为CO32-+H2O?HCO3-+OH-,
故答案为:CO32-+H2O?HCO3-+OH-;
(3)M为(NH4)2CO3 或NH4HCO3,含有的阳离子为铵根离子,实验室检验铵根离子,可加入氢氧化钠溶液共热,产生能使湿润的红色石蕊试纸变蓝的气体,则证明NH4+存在,
故答案为:加入氢氧化钠溶液共热,产生能使湿润的红色石蕊试纸变蓝的气体,则证明NH4+存在;
(4)G到E是铜和稀硝酸反应生成硝酸铜、一氧化氮和水,离子方程式为:3Cu+8H++2N03-=3Cu2++2NO↑+4H2O,每生成标况下1.12L的NO,即0.05mol,则转移电子的物质的量为0.05mol×(5-2)=0.15mol,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;0.15.
(1)由上述分析可知,M为(NH4)2CO3 或NH4HCO3,F为NO2,
故答案为:NH4HCO3(或(NH4)2CO3);NO2;
(2)反应①除生成氧气外,生成的另一种物质为碳酸钠,碳酸钠为强碱弱酸盐,水解呈碱性,离子方程式为CO32-+H2O?HCO3-+OH-,
故答案为:CO32-+H2O?HCO3-+OH-;
(3)M为(NH4)2CO3 或NH4HCO3,含有的阳离子为铵根离子,实验室检验铵根离子,可加入氢氧化钠溶液共热,产生能使湿润的红色石蕊试纸变蓝的气体,则证明NH4+存在,
故答案为:加入氢氧化钠溶液共热,产生能使湿润的红色石蕊试纸变蓝的气体,则证明NH4+存在;
(4)G到E是铜和稀硝酸反应生成硝酸铜、一氧化氮和水,离子方程式为:3Cu+8H++2N03-=3Cu2++2NO↑+4H2O,每生成标况下1.12L的NO,即0.05mol,则转移电子的物质的量为0.05mol×(5-2)=0.15mol,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;0.15.
点评:本题考查无机物的推断,为高频考点,侧重于学生的分析能力的考查,A、C为解答本题的突破口,然后利用转化关系推出各物质是解答本题的关键,题目难度中等.

练习册系列答案
相关题目
某有机物完全燃烧只生成CO2和H2O,两者的物质的量之比为2:3,可以说( )
| A、该有机物中含C、H、O三种原子 |
| B、该化合物是乙烷 |
| C、该化合物中C、H原子个数比为1:3 |
| D、该化合物分子中含2个C原子、6个H原子,但一定不含有O原子 |
工业生产中常将两种或多种金属(或金属与非金属)在同一容器中加热使其熔合,冷凝后得到具有金属特性的熔合物--合金.这是制取合金的常用方法之一.根据下表数据判断,不宜用上述方法制取合金的是( )
| 金属 | Na | Al | Cu | Fe |
| 熔点(℃) | 97.81 | 660 | 1083 | 1535 |
| 沸点(℃) | 883 | 2200 | 2595 | 3000 |
| A、Fe-Cu合金 |
| B、Cu-Al合金 |
| C、Al-Na合金 |
| D、Cu-Na合金 |
经测定C3H7OH和C6H12组成的混合物中碳的质量分数为78%,则此混合物中氧的质量分数是( )
| A、8% | B、10% |
| C、22% | D、18% |
下列说法中正确的是( )
| A、所有主族元素的正化合价数,等于它的族序数 |
| B、第ⅦA族元素的原子随核电荷数的增加,得电子能力逐渐减弱 |
| C、第ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布 |
| D、前三周期元素中共有非金属元素12种 |
 在一定条件下,物质A~E相互转化的关系下图所示,其中A为单质,常温下E是无色液体.请根据条件回答下列问题(填写化学用语):
在一定条件下,物质A~E相互转化的关系下图所示,其中A为单质,常温下E是无色液体.请根据条件回答下列问题(填写化学用语):