题目内容
1. 某实验小组用如图所示装置进行实验以探究Fe3+、Cl2和SO2的氧化性强弱(夹持仪器已略).
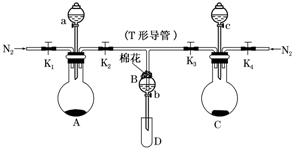
某实验小组用如图所示装置进行实验以探究Fe3+、Cl2和SO2的氧化性强弱(夹持仪器已略).(1)按图连接好装置,检查A装置的气密性的方法为
关闭a、b、K1、K3,打开K2,向B装置中加水,将T形导管下端插入水中,微热A装置,看到有气泡产生,停止加热恢复室温,T形导管下端形成一段水柱,说明A装置气密性良好.
(2)检查完装置的气密性,添加药品,向A装置的分液漏斗中加入浓盐酸,在圆底烧瓶中加入固体KMnO4;向B装置中加入10mL FeCl2溶液;在C装置的分液漏斗中加入70%的硫酸,向圆底烧瓶中加入固体Na2SO3;棉花浸润NaOH溶液.打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2,然后关闭K1,K3,K4.通入一段时间N2的目的是排出装置中的空气,防止其干扰实验.
(3)打开活塞a,逐滴加入浓盐酸,当B中溶液变为棕黄色时,停止滴加浓盐酸,夹紧K2,打开活塞b,使约2mL的溶液流入D试管中,分别取1mL溶液滴入硫氰化钾(填试剂名称)和铁氰化钾溶液可以证明其中含有Fe3+和Fe2+.A装置中发生反应的离子方程式为2MnO4-+10Cl-+16H+═2Mn2++5Cl2↑+8H2O.
(4)打开K3和活塞c,逐滴加入70%的硫酸,当B中溶液颜色逐渐变为浅绿色,停止滴加70%的硫酸,夹紧K3,打开活塞b,使约2mL的溶液流入D试管中,并检验其中的离子.B中发生反应的离子方程式为SO2+2Fe3++2H2O═2Fe2++SO42-+4H+.
(5)结合实验现象判断Fe3+、Cl2、SO2氧化性由弱到强的顺序为SO2<Fe3+<Cl2.
分析 (1)检查装置气密性,首先要密闭,应关闭a、b、K1、K3,打开K2,向B装置中加水,T形导管下端插入水中,微热A装置,根据是否看到气泡及停止加热恢复室温,T形导管下端是否形成一段水柱进行判断;
(2)氯气、二氧化硫有毒,需要用用碱溶液吸收;装置中氧气干扰实验,则通入一段时间N2的目的排出装置中的空气;
(3)氯气将氯化亚铁中的Fe2+氧化为Fe3+,可用硫氰化钾可以证明其中含有Fe3+;A装置中氯离子被酸性高锰酸根离子氧化成氯气,据此写出反应的离子方程式;
(4)Fe3+被SO2还原为Fe2+,亚铁离子的溶液为浅绿色;B中铁离子将二氧化硫氧化成硫酸,据此写出离子方程式;
(5)结合实验现象及氧化还原反应原理判断Cl2、Fe3+和SO2的氧化性由弱到强的顺序.
解答 解:(1)检查装置气密性,首先要密闭,应关闭a、b、K1、K3,打开K2,向B装置中加水,T形导管下端插入水中,微热A装置,看到有气泡产生,停止加热恢复室温,T形导管下端形成一段水柱,说明A装置气密性良好,
故答案为:关闭a、b、K1、K3,打开K2,向B装置中加水,将T形导管下端插入水中,微热A装置,看到有气泡产生,停止加热恢复室温,T形导管下端形成一段水柱,说明A装置气密性良好;
(2)用碱溶液吸收多余的氯气、二氧化硫,防止污染空气;通入一段时间N2的目的是排出装置中的空气,防止其干扰实验,
故答案为:NaOH;排出装置中的空气,防止其干扰实验;
(3)氯气将氯化亚铁中的Fe2+氧化为Fe3+,Fe3+遇KSCN溶液变为血红色,则用硫氰化钾可以证明其中含有Fe3+;A装置中酸性条件下高锰酸根离子将氯离子氧化成氯气,反应的离子方程式为:2MnO4-+10Cl-+16H+═2Mn2++5Cl2↑+8H2O,
故答案为:硫氰化钾;2MnO4-+10Cl-+16H+═2Mn2++5Cl2↑+8H2O;
(4)Fe3+被SO2还原为Fe2+,溶液变为浅绿色;B中二氧化硫被铁离子氧化成硫酸,反应的离子方程式为:SO2+2Fe3++2H2O═2Fe2++SO42-+4H+,
故答案为:浅绿;SO2+2Fe3++2H2O═2Fe2++SO42-+4H+;
(5)结合实验现象及氧化还原反应原理可知:Cl2、Fe3+和SO2的氧化性由弱到强的顺序为:SO2<Fe3+<Cl2,
故答案为:SO2<Fe3+<Cl2.
点评 本题考查了性质实验方案的设计,题目难度中等,涉及氧化还原反应中氧化性、还原性强弱判断、化学实验基本操作方法应用、性质方案设计与评价等知识,明确实验目的及反应原理为解答关键,试题培养了学生的分析能力及化学实验能力.

 阅读快车系列答案
阅读快车系列答案| A. | NaOH(s) | B. | CH3COONa(s) | C. | FeCl3(s) | D. | NH4Cl |
| A. | 16g | B. | 8g | C. | 40g | D. | 0.2mol |
| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) |
| 乙醇 | -117.3 | 78.5 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | 338.0 | 1.84 |
①在30mL的大试管A中按体积比2:3:3配制浓硫酸、乙醇和乙酸的混合溶液.
②按图1连接好装置(装置气密性良好),用小火均匀加热装有混合液的大试管5~10min.
③待试管B收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置.
请根据题目要求回答下列问题:
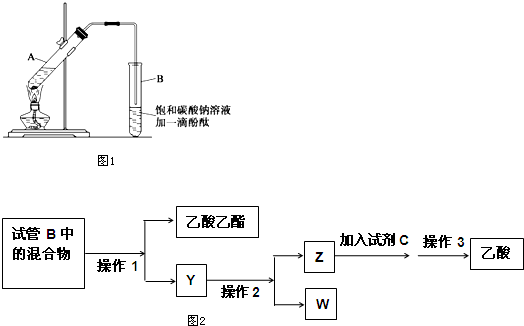
(1)配制该混合液时,滴加药品的顺序是乙醇,浓硫酸、乙酸(乙醇和浓硫酸的加入顺序不可互换).
(2)浓硫酸的主要作用是催化剂、脱水剂.
(3)导管不能插入到Na2CO3溶液中的原因是防止倒吸.
(4)做此实验时,有时还向A试管里加入几块碎瓷片,其目的是防止暴沸.
(5)指出步骤③所观察到的现象:液体分层,上层有无色油状液体,下层液体红色变浅.
(Ⅱ)实验完成后,图2是对图1试管B中收集到的混合物进行分离操作步骤流程图:
请回答:
(6)操作1,操作2,操作3所对应的操作名称为分液、蒸馏、蒸馏.
(7)得到的物质W中的官能团名称为羟基.
(8)试剂C可以选用下列的A(填序号).
A.H2SO4 B.CO2 C.NaOH D.NaCl.
| A. | 纯净物C4H8的核磁共振氢谱峰最多为4 | |
| B. | 化学式为C8H8的有机物,一定能使酸性高锰酸钾溶液褪色 | |
| C. | 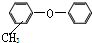 的同分异构体中,可以有醇、酚类物质 的同分异构体中,可以有醇、酚类物质 | |
| D. | 1 mol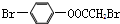 最多能与2 mol NaOH反应 最多能与2 mol NaOH反应 |
| A. | 蛋白质、纤维、油脂、淀粉、聚乙烯都是高分子化合物 | |
| B. | 蛋白质的水解产物为氨基酸 | |
| C. | 使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 | |
| D. | 石油、煤、天然气、可燃冰、植物油都属于化石燃料 |
