题目内容
13.已知下表所示数据:| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) |
| 乙醇 | -117.3 | 78.5 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | 338.0 | 1.84 |
①在30mL的大试管A中按体积比2:3:3配制浓硫酸、乙醇和乙酸的混合溶液.
②按图1连接好装置(装置气密性良好),用小火均匀加热装有混合液的大试管5~10min.
③待试管B收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置.
请根据题目要求回答下列问题:
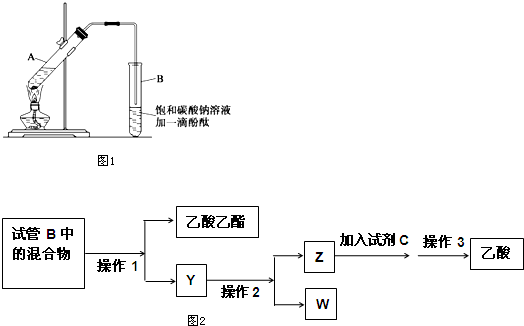
(1)配制该混合液时,滴加药品的顺序是乙醇,浓硫酸、乙酸(乙醇和浓硫酸的加入顺序不可互换).
(2)浓硫酸的主要作用是催化剂、脱水剂.
(3)导管不能插入到Na2CO3溶液中的原因是防止倒吸.
(4)做此实验时,有时还向A试管里加入几块碎瓷片,其目的是防止暴沸.
(5)指出步骤③所观察到的现象:液体分层,上层有无色油状液体,下层液体红色变浅.
(Ⅱ)实验完成后,图2是对图1试管B中收集到的混合物进行分离操作步骤流程图:
请回答:
(6)操作1,操作2,操作3所对应的操作名称为分液、蒸馏、蒸馏.
(7)得到的物质W中的官能团名称为羟基.
(8)试剂C可以选用下列的A(填序号).
A.H2SO4 B.CO2 C.NaOH D.NaCl.
分析 (Ⅰ)(1)从浓硫酸溶于水放热和加热时试管内液体的体积不超过试管容积的“13”分析,加入药品时,为防止酸液飞溅,应先加入乙醇再加入浓硫酸和乙酸;
(2)乙酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;
(3)根据粗产品乙酸乙酯、乙酸和乙醇的混合物中各自的性质,以及加热不充分也能产生倒吸进行解答;
(4)乙酸、乙醇沸点低,液体加热要加碎瓷片,防止暴沸;
(5)根据乙酸的酸性和乙酸乙酯难溶于饱和碳酸钠分析;
(Ⅱ)(6)分离互不相溶的液体,可用分液的方法分离;分离沸点不同且互溶的液体用蒸馏操作;
(7)得到的物质W为乙醇,根据乙醇的结构解答;
(8)Z中的乙酸钠与强酸反应生成乙酸;
解答 解:(1)浓硫酸溶于水放出大量的热,乙醇中含有少量水,应将浓硫酸加入到乙醇中,防止硫酸溶解时放出大量的热导致液体飞溅,另外,加热时,试管内液体的体积不超过试管容积的“13”,加入药品的顺序为在一个30mL大试管中注入3mL乙醇,再分别缓缓加入2mL浓硫酸和3mL乙酸(乙酸和浓硫酸的加入顺序可互换),边加边振荡试管使之混合均匀(药品总用量不能超过10mL),
故答案为:乙醇,浓硫酸、乙酸(乙醇和浓硫酸的加入顺序不可互换);
(2)乙酸与乙醇发生酯化反应,该反应为可逆反应,需浓硫酸作催化剂,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,故浓硫酸的作用为催化剂、吸水剂,
故答案为:催化剂、脱水剂;
(3)乙酸乙酯中混有乙醇和乙酸,二者易溶于水而产生倒吸,加热不充分也能产生倒吸,导管不能插入到Na2CO3溶液中,防止倒吸回流现象的发生,
故答案为:防止倒吸;
(4)乙酸、乙醇沸点低,液体加热要加碎瓷片,引入汽化中心,可防止溶液暴沸,
故答案为:防止暴沸;
(5)碳酸钠水解呈碱性,乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,有香味,所以克观察到液体分层,上层有无色油状液体,振荡时乙酸和碳酸钠反应而使溶液红色变浅,
故答案为:液体分层,上层有无色油状液体,下层液体红色变浅;
(6)分离乙酸乙酯时先将盛有混合物的试管充分振荡,让饱和碳酸钠溶液中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,静置分层后取上层得乙酸乙酯,所以操作1为分液,Y为乙酸钠、碳酸钠和乙醇的混合溶液,分离沸点不同且互溶的液体用蒸馏操作,所以操作2为蒸馏分离出乙醇,乙酸钠、碳酸钠加入强酸,操作3为蒸馏出乙酸,
故答案为:分液;蒸馏;蒸馏;
(7)Y为乙酸钠、碳酸钠和乙醇的混合溶液,乙醇的沸点较低,因此W为乙醇,乙醇含有官能团羟基,
故答案为:羟基
(8)根据强酸制弱酸的原理,Z中的乙酸钠与硫酸反应方可生成乙酸,
故答案为:A.
点评 本题考查乙酸乙酯的制备,涉及酯化反应的制备反应装置,反应条件,反应特征等分析判断、分离混合物的操作步骤和方法选择和实验评价的分析等方面,题目难度中等.

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案| A. | HX、HZ、HY | B. | HY、HZ、HX | C. | HZ、HY、HX | D. | HX、HY、HZ |
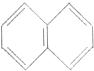 ,若萘分子中有两个氢原子分别被溴原子取代,所形成的化合物的数目有( )
,若萘分子中有两个氢原子分别被溴原子取代,所形成的化合物的数目有( )| A. | 5种 | B. | 7种 | C. | 8种 | D. | 10种 |
| A. | 甲烷分子的比例模型是: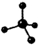 | B. | 二氧化碳的电子式: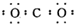 | ||
| C. | CO2的比例模型: | D. | HClO的结构式为:H-O-Cl |
| A. | 常见铅蓄电池放电时,负极质量减轻,正极质量增加 | |
| B. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| C. | 常温下,pH=5的盐酸稀释1000倍后,溶液的pH=8 | |
| D. | 水的离子积随温度升高而增大,说明水的电离是吸热反应 |
| A. | 乙烯通入溴水中 | B. | 光照射甲烷与氯气的混合气体 | ||
| C. | 苯与液溴混合后撒入铁粉 | D. | 乙酸和乙醇在浓硫酸作用下酯化 |
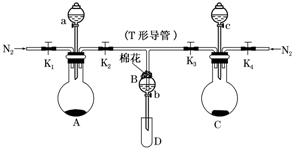 某实验小组用如图所示装置进行实验以探究Fe3+、Cl2和SO2的氧化性强弱(夹持仪器已略).
某实验小组用如图所示装置进行实验以探究Fe3+、Cl2和SO2的氧化性强弱(夹持仪器已略). 目前工业上制备丙烯腈(CH2=CHC≡N)有乙炔法、丙烯氨氧化法等.
目前工业上制备丙烯腈(CH2=CHC≡N)有乙炔法、丙烯氨氧化法等.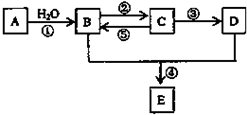 A、B、C、D、E(部分反应条件、产物被省略).其中A是一种重要的化工材料,它的产量可以用来衡量一个国家的石油化工水平;B和D式生活中两种常用的有机物;E是具有果香气味的烃的衍物.
A、B、C、D、E(部分反应条件、产物被省略).其中A是一种重要的化工材料,它的产量可以用来衡量一个国家的石油化工水平;B和D式生活中两种常用的有机物;E是具有果香气味的烃的衍物.