题目内容
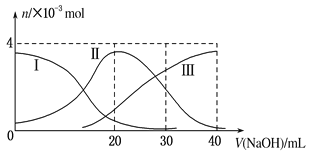
【题目】根据如图能量关系示意图,下列说法正确的是( )
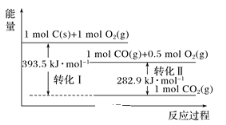
A.1molC(s)与1 molO2(g)的能量之和为393.5kJ
B.反应2CO(g)+O2(g)=2CO2(g)中,生成物的总能量大于反应物的总能量
C.由C(s)→CO(g)的热化学方程式为:2C(s)+O2(g)= 2CO(g) ΔH=-221.2kJ·mol-1
D.CO的燃烧热ΔH=-282.9kJ
【答案】C
【解析】
A. 1molC(s)与1 molO2(g)反应变成1mol二氧化碳气体,放出的能量为393.5kJ ,不能说明碳和氧气的能量和就是393.5kJ,故错误;
B. 反应2CO(g)+O2(g)=2CO2(g)为放热反应,故生成物的总能量小于反应物的总能量,故错误;
C. 根据图示可以分析,有①C(s)+O2(g)= CO2 (g) ΔH=-393.5kJ·mol-1, ②CO(g)+![]() O2(g)= CO2(g) ΔH=-282.9kJ·mol-1,故根据盖斯定律分析,①-②得C(s)→CO(g)的热化学方程式C(s)+
O2(g)= CO2(g) ΔH=-282.9kJ·mol-1,故根据盖斯定律分析,①-②得C(s)→CO(g)的热化学方程式C(s)+![]() O2(g)= CO(g) ΔH=-393.5+282.9=-110.6kJ·mol-1,可写成2C(s)+O2(g)= 2CO(g) ΔH=-221.2kJ·mol-1,故正确;
O2(g)= CO(g) ΔH=-393.5+282.9=-110.6kJ·mol-1,可写成2C(s)+O2(g)= 2CO(g) ΔH=-221.2kJ·mol-1,故正确;
D.燃烧热的单位为kJ·mol-1,故错误。
故选C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目