题目内容
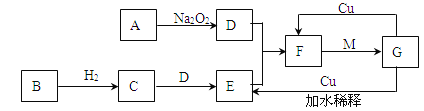
【题目】某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色胶状沉淀,I为红褐色沉淀。(此转化关系中所用的试剂都是足量的)
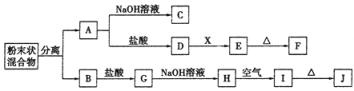
(1)写出下列物质的化学式:F____________,G________________。
(2)将混合物中两种金属分离开的最简单的方法是___________。
(3)D→E的转化中,加入过量的X可能是_____________________。
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)写出下列转化的化学方程式:
A→C:______________________________________________;
H→I:_______________________________________________。
【答案】Al2O3 FeCl2 用磁铁靠近粉末状混合物,将铁粉吸附在磁铁表面 C 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】
I为红褐色沉淀判断为Fe(OH)3,加热反应生成J为Fe2O3,H在空气中氧化为氢氧化铁推断H为Fe(OH)2,B+HCl=G,推断G为FeCl2,B为Fe,含A、B两种金属单质的粉末状混合物中B为Fe,A能和氢氧化钠反应、盐酸反应说明为Al,所以C为NaAlO2,D为AlCl3,依据E为白色沉淀Al(OH)3,则X为制备氢氧化铝的反应最好选择氨水,则X为NH3H2O,F为Al2O3,依据推断物质分析回答问题。
(1)依据判断F、G的化学式为:F为Al2O3,G为FeCl2;
(2)混合物中两种金属分离开的最简单的方法是利用铁可以被磁铁吸引,方法为:用磁铁靠近粉末状混合物,将铁粉吸附在磁铁表面;
(3)D→E的转化中是X和氯化铝反应生成氢氧化铝的反应,依据实验室制取氢氧化铝的方法和氢氧化铝的性质分析,氢氧化铝能溶于过量强碱溶液中,所以加入过量的X可能是氨水,故答案为:C;
(4)A→C是Al和氢氧化钠反应生成偏铝酸钠和氢气,反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;H→I是氢氧化亚铁被氧化为氢氧化铁,该反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3。

 阅读快车系列答案
阅读快车系列答案【题目】一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)。各容器中起始物质的量浓度与反应温度如下表所示:
N2(g)+2CO2(g)。各容器中起始物质的量浓度与反应温度如下表所示:
容器 | 温度/℃ | 起始物质的量浓度/(mol·L-1) | |||
NO(g) | CO(g) | N2 | CO2 | ||
甲 | T1 | 0.10 | 0.10 | 0 | 0 |
乙 | T2 | 0 | 0 | 0.10 | 0.20 |
丙 | T2 | 0.10 | 0.10 | 0 | 0 |
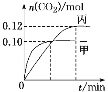
反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示。下列说法正确的是
A.该反应的正反应为放热反应,平衡常数K(T1)<K(T2)
B.乙容器中反应达到平衡时,N2的转化率小于40%
C.达到平衡时,乙容器中的压强一定大于甲容器的2倍
D.丙容器中反应达到平衡后,再充入0.10 mol NO和0.10 mol CO2,此时υ(正)<υ(逆)