题目内容
定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO12.0g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则V可能为( )
| A.9.0L | B.13.5L | C.15.7L | D.16.8L |
A
解析试题分析:由铜守恒可知CuS与Cu2S中含有n(Cu)=12.0g/80g·mol-1=0.15mol,利用电子守恒,依据“极端假设法”可知,当混合物全部为CuS时可得:0.15mol×8=n(NO)×3+n(NO2) ×1,因n(NO)=n(NO2),解之得n(NO)=n(NO2)=0.3mol,则反应所得混合气体在标况下的体积V=(0.3mol+0.3mol)×22.4mol·L-1=13.44L;当混合物全部为Cu2S时可得:
10×0.15mol/2=n(NO)×3+n(NO2) ×1
因n(NO)=n(NO2),解之得n(NO)=n(NO2)=0.1875mol,则反应所得混合气体在标况下的体积V=(0.1875mol+0.1875mol)×22.4mol·L-1=8.4L,所以收集到气体体积:8.4L<V<13.44L,故选A。
考点:化学计算

 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案在反应3Cl2+8 NH3 = N2+6NH4Cl中,氧化剂与还原剂的物质的量之比为( )
| A.8:3 | B.3:8 | C.3:2 | D.1:3 |
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是( )
| A.2Al+2NaOH+2H2O=2NaAlO2+3H2↑ |
| B.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| C.BrCl+H2O=HCl+HbrO |
| D.2Na2O2+2H2O=4NaOH+O2↑ |
某含Cr2O72-废水用硫酸亚铁铵[(NH4)2 Fe(SO4)2?6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀干燥后得到n molFeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述正确的是
| A.反应中转移的电子总数为3nx mol |
| B.Cr2O72-转化为沉淀时被氧化 |
| C.消耗硫酸亚铁铵的物质的量为n(2-x)mol |
| D.在FeO?FeyCrxO3中3y=x |
锑(Sb)在自然界一般以硫化物的形式存在,我国锑的蕴藏量为世界第一,从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原:
①2Sb2S3+3O2+6Fe Sb4O6+6FeS②Sb4O6+6C
Sb4O6+6FeS②Sb4O6+6C 4Sb+6CO↑,关于反应①、②的说法正确的是( )
4Sb+6CO↑,关于反应①、②的说法正确的是( )
A.反应①②中的氧化剂分别是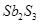 、 、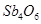 |
| B.反应①中每生成1mol FeS时,共转移3mol电子 |
| C.反应②说明高温下C的还原性比Sb强 |
| D.每生成4mol Sb时,反应①与反应②中还原剂的物质的量之比为4:3 |
将0.195g锌粉加入到20mL 0.100 mol?L-1MO2+溶液中,恰好完全反应,则还原产物可能是
| A.M | B.M2+ | C.M3+ | D.MO2+ |
已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是( )
| A.上述实验证明氧化性:MnO4->Cl2>Fe3+>I2 |
| B.上述实验中,共有两个氧化还原反应 |
| C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝 |
| D.实验②证明Fe2+既有氧化性又有还原性 |
三氟化氮是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:
3NF3+5H2O=2NO+HNO3+9HF。下了有关该反应的说法正确的是:
| A.NF3是氧化剂,H2O是还原剂 |
| B.还原剂与氧化剂的物质的量之比为2:1 |
| C.若生成0.2mol HNO3,则转移0.2mol电子 |
| D.NF3在潮湿的空气中泄漏会产生红棕色气体 |