题目内容
4.下列有关化学用语的表述错误的是( )| A. | Ca2+的结构示意图为: | |
| B. | 氯仿的化学式:CHCl3 | |
| C. | R2+离子核外有a个电子,b个中子,R原子表示为a+ba+b+2R | |
| D. | 溴化氢分子的电子式: |
分析 A.钙离子的核电荷数为20,核外电子总数为18,最外层达到8电子稳定结构;
B.氯仿为三氯甲烷,可以看作甲烷分子中3个H被氯原子取代后生成的;
C.元素符合左下角的数字表示质子数,左上角数字表示质量数;
D.溴化氢为共价化合物,分子中不存在阴阳离子.
解答 解:A.Ca2+的核外电子总数为18,最外层为8个电子,其离子结构示意图为: ,故A正确;
,故A正确;
B.三氯甲烷又名氯仿,其分子式为CHCl3,故B正确;
C.R2+离子核外有a个电子,b个中子,则R原子的质子数为a+2,质量数为a+b+2,R原子符号为:a+ba+b+2R,故C正确;
D.溴化氢属于共价化合物,分子中不存在阴阳离子,溴化氢正确的电子式为: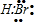 ,故D错误;
,故D错误;
故选CD.
点评 本题考查了化学用语的表示方法判断,题目难度中等,注意掌握离子结构示意图、元素符号、结构式、电子式的概念及书写原则,试题培养了学生规范答题的能力.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
15.下列说法中,正确的是( )
| A. | 氧气和臭氧互为同分异构体 | B. | 二氧化碳晶体中存在分子间作用力 | ||
| C. | 1H2O和2H2O互为同位素 | D. | 正丁烷和异丁烷互为同系物 |
19.共价化合物含C、H、N三种元素.分子内有四个N原子,成四面体;每两个N原子之间都含有1个C原子.又知分子中无C一C键和C=C键,该化合物的分子式( )
| A. | C3H8N4 | B. | C6H12N4 | C. | C6H10N4 | D. | C4H8N4 |
9.可用自由电子与金属离子的碰撞中有能量传递来解释的物理性质是( )
| A. | 金属是热的良导体 | B. | 金属是电的良导体 | ||
| C. | 金属有良好的延展性 | D. | 有金属光泽,不透明 |
16.元素电负性随原子序数的递增而增强的是( )
| A. | Na、K、Rb | B. | N、P、As | C. | Si、P、Cl | D. | O、S、Cl |
13.如图所示的装置中,能够组成原电池,产生电流的是( )
| A. |  | B. | 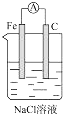 | C. |  | D. | 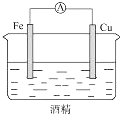 |
 将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol•L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol•L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示: 物质的结构决定性质,性质反映其结构特点.
物质的结构决定性质,性质反映其结构特点.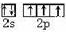 .
.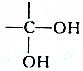 结构的有机物不能稳定存在,根据以上信息,试回答:
结构的有机物不能稳定存在,根据以上信息,试回答: +2H2O,是酯化反应.
+2H2O,是酯化反应.