题目内容
11.科学合理的综合利用海水资源,是开发和利用自然资源的重要方面.下列不需要化学变化就能够从水中获得的物质是( )| A. | 氯、溴、碘 | B. | 食盐、淡水 | C. | 烧碱、氢气 | D. | 钠、镁、铝 |
分析 据从海水制备物质的原理可知,金属单质与非金属单质需要利于化学反应来制取,而食盐可利用蒸发原理,淡水利用蒸馏原理来得到.
解答 解:A.可从海水中获得氯化钠,通过电解熔融氯化钠得到钠和氯气,是化学变化,通过氯气将溴离子和碘离子氧化为溴单质和碘单质,是化学变化,故A错误;
B.把海水用蒸馏等方法可以得到淡水,把海水经太阳暴晒,蒸发水分后即得食盐,不需要化学变化就能够从海水中获得,故B正确;
C.可从海水中获得氯化钠,配制成饱和食盐水,然后电解,即得烧碱、氢气和氯气,是化学变化,故C错误;
D.可从海水中获得氯化钠,电解熔融氯化钠得到钠和氯气,是化学变化,通过电解熔融的氯化镁和氧化铝即得镁和铝,是化学变化,故D错误;
故选B.
点评 本题考查了海水的成分,海水提炼氯气、溴、碘、钠、镁、氢气等物质的原理,难度不大,掌握原理是解题的关键.

练习册系列答案
相关题目
1.已知:
(1)工业制镁时,电解MgCl2而不电解MgO的原因是MgO的熔点比MgCl2的熔点高,MgO熔融时耗费更多能源,增加成本;
(2)制铝时,电解Al2O3而不电解AlCl3的原因是是共价化合物,熔融态时不电离,难导电.
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2 800 | 2 050 | 714 | 191 |
(2)制铝时,电解Al2O3而不电解AlCl3的原因是是共价化合物,熔融态时不电离,难导电.
19.下列各项表述中正确的是( )
| A. | Na2O2中阴离子和阳离子数目比为1:1 | |
| B. | 任何离子键的形成过程都有电子的得失 | |
| C. | 已知C(石墨)=C(金刚石)是吸收能量的反应,由此说明石墨比金刚石稳定 | |
| D. | 通过测量AlCl3溶液的导电性,可判断其为共价化合物 |
16.下列关于硫及含硫化合物的叙述正确的是( )
| A. | SO2的漂白原理与次氯酸相同 | |
| B. | 硫在空气中燃烧生成大量SO3 | |
| C. | 金属钠应保存在水里以隔绝空气 | |
| D. | 常温下铝遇浓硫酸钝化,因此可用铝槽储运浓硫酸 |
3.乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,反应可表示为CH2=C=O+HA→CH3-CO-A.乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是( )
| A. | 与HCl加成生成CH3COCl | B. | 与H2O加成生成CH3COOH | ||
| C. | 与CH3COOH加成生成CH3COOCOCH3 | D. | 与CH3OH加成生成CH3COCH2OH |
1.下列反应中,硫酸不作氧化剂的是( )
| A. | 2HBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Br2+SO2↑+2H2O | |
| B. | Ca3(PO4)2+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2CaSO4+Ca(H2PO4)2 | |
| C. | 2Al+3H2SO4═Al2(SO4)3+3H2↑ | |
| D. | 2KMnO4+5H2S+3H2SO4═K2SO4+2MnSO4+5S↓+8H2O |
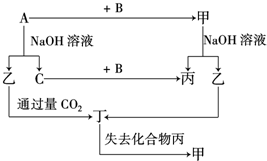 由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有如图所示的转换关系,已知C为密度最小的气体,甲是电解质.
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有如图所示的转换关系,已知C为密度最小的气体,甲是电解质. .
.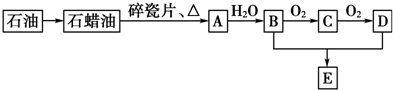
 ,它的一氯取代产物有2种.
,它的一氯取代产物有2种.