题目内容
【题目】下列有关实验原理或实验操作正确的是
A.用水湿润的pH试纸测量某溶液的pH
B.用量筒量取20 mL0.5000 mol·L-1 H2SO4溶液于烧杯中,加水80mL,配制成0.1000 mol· L-1H2SO4溶液
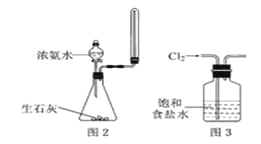
C.实验室用图2所示装置制取少量氨气
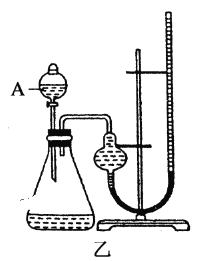
D.实验室用图3所示装置除去Cl2中的少量HCl
【答案】D
【解析】
A.用水润湿的pH试纸,溶液稀释,则测定pH时试纸不能润湿,故A错误;
B.配制80mL0.1000 molL-1H2SO4溶液需要100mL容量瓶,应在烧杯中稀释、冷却后转移到容量瓶中定容,故B错误;
C.收集氨气的试管口不能密封,可塞一团棉花,故C错误;
D.HCl极易溶于水,食盐水抑制氯气的溶解,则用图②所示装置除去Cl2中的少量HCl,故D正确;
故选D。
【点晴】
把握相关物质的性质、实验操作、实验技能为解答的关键。解答此类试题的基本流程:原理→反应物质→仪器装置→现象→结论→作用意义→联想。具体分析为:①实验是根据什么性质和原理设计的?实验的目的是什么?②所用各物质名称、状态、代替物(根据实验目的和相关的化学反应原理,进行全面的分析比较和推理,并合理选择)。③有关装置:性能、使用方法、适用范围、注意问题、是否有替代装置可用、仪器规格等。④有关操作:技能、操作顺序、注意事项或操作错误的后果。⑤实验现象:自下而上,自左而右全面观察。⑥实验结论:直接结论或导出结论。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案【题目】确定物质性质的重要因素是物质结构。请回答下列问题。
(1)A、B、C、D为四种晶体,性质如下:
A.固态、液态时均不导电,熔点-120 ℃,能溶于CS2
B.固态、液态时大多不导电,硬度很大,熔点为3500 ℃
C.固态和熔融态时都能导电,能溶于盐酸
D.固态时不导电,液态时能导电,可溶于水
试推断它们的晶体类型:
A.______; B.______; C._____; D._____。
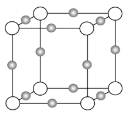
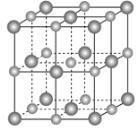
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如下图所示,其中TiN中N呈-3价),已知其中3种离子晶体的晶格能数据如下表:
离子晶体 | KCl | MgO | CaO |
晶格能/kJ·mol-1 | 715 | 3791 | 3401 |
则该4种离子晶体的熔点从高到低的顺序是______。
(3)某离子X+中所有电子正好充满K、L、M三个电子层,它与N3-形成晶体的结构如下图所示。X的元素名称是_____,X+的价电子排布式为_____,与同一个N3-相连的X+有_____个,这几个X+所形成的空间构型为_____。