题目内容
【题目】常温下,用 0.1000 mol·L![]() NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L![]()
![]() 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是
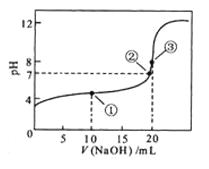
A.点①所示溶液中:![]()
B.点②所示溶液中:![]()
C.点③所示溶液中:![]()
D.滴定过程中可能出现:![]()
【答案】D
【解析】
A、点①反应后溶液是CH3COONa与CH3COOH物质的量之比为1:1的混合物,CH3COOH电离程度大于CH3COO-的水解程度,故c(Na+)>c(CH3COOH),由电荷守恒可知: c(CH3COO-)+c(OH-)=c(Na+)+c(H+),所以c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+),故A错;
B、点②pH=7,即c(H+)=c(OH-),由电荷守恒知:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),故c(Na+)=c(CH3COO-),故B错;
C、点③说明两溶液恰好完全反应生成CH3COONa,由于CH3COO-水解,且程度较小,所以c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故C错;
D、当CH3COOH较多,滴入的碱较少时,则生成CH3COONa少量,可能出现c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-),故D正确,答案选D。

 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【题目】一定条件下可利用甲烷消除氮氧化物的污染,例如:CH4+2NO2N2+CO2+2H2O。在2L密闭容器中,控制在不同温度下,分别加入0.50molCH4和0.90molNO2,测得n(CH4)随时间变化的有关实验数据如下表所示。
组别 | 温度 | n/mol | 时间/min | ||||
0 | 10 | 20 | 40 | 50 | |||
① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | x | 0.15 |
下列说法不正确的是
A.组别①中,0~20min内,NO2的降解速率为0.025mol·L-1·min-1
B.该反应的△H<0
C.40min时,x的数值应为0.15
D.0~20min内NO2的降解百分数①<②