题目内容
【题目】化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素的最外层p轨道上的电子数等于前一电子层电子总数;X原子最外层的p轨道中有一个轨道填充了2个电子。则
(1)X元素基态原子的电子排布式是________,Y原子的价层电子的电子排布图是_________。
(2)YX2的分子构型是____________。
(3)YX2分子中,Y原子的杂化类型是__________,一个YX2分子中含________个π键。
【答案】 1s22s22p4 ![]() 直线形 sp杂化 2
直线形 sp杂化 2
【解析】试题分析:本题考查元素的推断,原子核外电子排布式和价层电子排布图的书写,分子空间构型的判断,π键的确定。Y元素的最外层p轨道上的电子数等于前一电子层电子总数,Y为C元素;X、Y、Z都是前三周期元素,Y与Z同主族,Z为Si元素;X原子最外层的p轨道中有一个轨道填充了2个电子,X的价电子排布式为ns2np4,X与Y同周期,X为O元素。
(1)X为O元素,O基态原子核外有8个电子,根据构造原理,O基态原子的电子排布式为1s22s22p4。Y为C元素,C原子的核外电子排布式为1s22s22p2,价层电子排布式为2s22p2,价层电子排布图为![]() 。
。
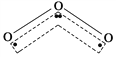
(2)YX2为CO2,CO2中C上的孤电子对数为![]() (4-2
(4-2![]() 2)=0,成键电子对数为2,C的价层电子对数为0+2=2,CO2的VSEPR模型为直线形,由于C上没有孤电子对,CO2的分子构型为直线形。
2)=0,成键电子对数为2,C的价层电子对数为0+2=2,CO2的VSEPR模型为直线形,由于C上没有孤电子对,CO2的分子构型为直线形。
(3)由于CO2中C的杂化轨道数为2,则其中C的杂化方式为sp杂化。CO2的结构式为O=C=O,1个CO2分子中含2个π键。

练习册系列答案
相关题目