题目内容
下列表述正确的是( )
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以先加硝酸溶液,再加氯化钡溶液来检验
③锌与稀硝酸反应可以得到氢气
④浓硫酸滴到纸张上变黑,说明浓硫酸具有吸水性
⑤二氧化硫和二氧化氮都能形成酸雨,酸雨的pH等于5.6.
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以先加硝酸溶液,再加氯化钡溶液来检验
③锌与稀硝酸反应可以得到氢气
④浓硫酸滴到纸张上变黑,说明浓硫酸具有吸水性
⑤二氧化硫和二氧化氮都能形成酸雨,酸雨的pH等于5.6.
| A、①③ | B、①② | C、① | D、①②④⑤ |
考点:硝酸的化学性质,氮的氧化物的性质及其对环境的影响,二氧化硫的化学性质,浓硫酸的性质
专题:元素及其化合物
分析:①依据浓硝酸具有不稳定性,见光易分解的性质解答;
②硝酸溶液具有强的氧化性,能够氧化亚硫酸根离子;
③稀硝酸具有强的氧化性,金属与硝酸反应得不到氢气;
④浓硫酸滴到纸张上变黑,体现其脱水性;
⑤酸雨的pH小于5.6.
②硝酸溶液具有强的氧化性,能够氧化亚硫酸根离子;
③稀硝酸具有强的氧化性,金属与硝酸反应得不到氢气;
④浓硫酸滴到纸张上变黑,体现其脱水性;
⑤酸雨的pH小于5.6.
解答:
解:①浓硝酸具有不稳定性,见光易分解,应该保存在棕色试剂瓶中,故正确;
②硝酸溶液具有强的氧化性,能够氧化亚硫酸根离子生成硫酸根离子,所以原溶液中是否含有硫酸根离子不能判断,故错误;
③硝酸具有强的氧化性,金属与硝酸反应得不到氢气,故错误;
④浓硫酸滴到纸张上变黑,体现其脱水性,故错误;
⑤酸雨的pH小于5.6,故错误;
故选:C.
②硝酸溶液具有强的氧化性,能够氧化亚硫酸根离子生成硫酸根离子,所以原溶液中是否含有硫酸根离子不能判断,故错误;
③硝酸具有强的氧化性,金属与硝酸反应得不到氢气,故错误;
④浓硫酸滴到纸张上变黑,体现其脱水性,故错误;
⑤酸雨的pH小于5.6,故错误;
故选:C.
点评:本题考查了浓硫酸、浓硝酸的性质,题目难度不大,熟悉浓硫酸、硝酸的性质是解题的关键,注意浓硫酸脱水性与吸水性的区别.

练习册系列答案
相关题目
下列说法正确的是( )
| A、向蒸馏水中滴加浓H2SO4时,KW不变 |
| B、常温下,0.005mol?L-1 Ba(OH)2溶液pH为12 |
| C、Na2CO3水解的离子方程式为:CO32-+2H2O?H2CO3+2OH- |
| D、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
有关化学键和化合物的叙述不正确的是( )
| A、盐酸中含有H+和Cl-,所以HCl是离子化合物 |
| B、Na2O2中含有离子键和非极性共价键 |
| C、完全由非金属元素组成的化合物可能是离子化合物 |
| D、双原子或多原子的单质分子中均存在化学键 |
化学与生活息息相关,下列说法正确的是( )
| A、二氧化硫可广泛的用于食品的漂白 |
| B、正常雨水的pH为7,酸雨的pH小于5.6 |
| C、煤经过气化和液化等物理变化可以转化为清洁燃料 |
| D、“地沟油”禁止食用,但可以用来制肥皂等 |
在2A+2B?C+5D反应中,表示该反应速率最快的是( )
| A、v(A)=0.5 mol/(L?s) |
| B、v(B)=0.3 mol/(L?s) |
| C、v(C)=0.4 mol/(L?s) |
| D、v(D)=1 mol/(L?s) |
设阿伏加德罗常数(NA)的数值为NA,下列说法正确的是( )
| A、1mol Cl2与足量Fe反应,转移的电子数为3NA |
| B、1.5mol NO2与足量H2O反应,转移的电子数为1.5NA |
| C、常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA |
| D、0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10NA |
关于淀粉的下列说法正确的是( )
| A、淀粉属于糖类,故有甜味 |
| B、用淀粉溶液可以检验单质碘的生成 |
| C、淀粉溶液中加少量稀硫酸作催化剂加热进行水解,冷却后再加银氨溶液可产生银镜 |
| D、淀粉与纤维素化学式均为(C6H10O5)n,故二者互为同分异构体 |
推断乙酰水杨酸(如图)不具有的化学性质( )
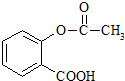

| A、与NaOH溶液反应 |
| B、水解反应 |
| C、与乙酸发生酯化反应 |
| D、与乙醇发生酯化反应 |