题目内容
16.由乙烯和乙醇蒸汽组成的混合气体中,碳的质量分数为60%.求氧的质量分数.分析 乙烯的分子式为C2H4,乙醇的分子式为C2H6O,可将乙醇的分子式看作C2H4•H2O,混合物可以看作C2H4、H2O的混合物,根据碳元素的质量百分含量可计算出C2H4的质量分数,进而计算的水质量分数,再计算氧元素的质量百分含量.
解答 解:乙烯的分子式为C2H4,乙醇的分子式为C2H6O,可将乙醇的分子式看作C2H4•H2O,混合物可以看作C2H4、H2O的混合物,混合物中ω(C)=60%,则ω(C2H4)=$\frac{60%}{\frac{24}{28}}$=70%,则ω(H2O)=1-70%=30%,所以:ω(O)=30%×$\frac{16}{18}$=26.7%,
答:氧元素的质量分数为26.7%.
点评 本题考查元素质量分数的计算,题目难度不大,注意利用分子式的转化,将乙醇的分子式可作C2H4•H2O.

练习册系列答案
相关题目
6.下列各化合物的命名中正确的是( )
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | B. | CH3-O-CH3乙醚 | ||
| C. |  | D. |  2-甲基丁烷 2-甲基丁烷 |
11.可逆反应A+3B?2C+2D,在不同条件下的反应,反应速率最快的是( )
| A. | vA=0.5mol/L•s | B. | vB=0.6mol/L•s | C. | vC=0.4mol/L•s | D. | vD=2mol/L•min |
5.既可以用来鉴别甲烷和乙烯,又可以用来除去乙烷中混有的乙烯,得到纯净乙烷的方法( )
| A. | 与足量酸性高锰酸钾反应 | B. | 依次通入通入足量溴水和浓硫酸中 | ||
| C. | 在一定条件下通入H2 | D. | 分别进行燃烧 |
6.下列电子式错误的是( )
| A. |  | B. |  | C. | 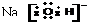 | D. |  |

 ,温度高于150℃完全分解得到固体Y和固体Z的化学方程式为4Na2SO3$\frac{\underline{\;高温\;}}{\;}$3Na2SO4+Na2S;
,温度高于150℃完全分解得到固体Y和固体Z的化学方程式为4Na2SO3$\frac{\underline{\;高温\;}}{\;}$3Na2SO4+Na2S;
 过碳酸钠(2Na2CO3•3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂,易分解.可用纯碱与H2O2反应制取,反应方程式为:2Na2CO3(aq)+3H2O2(aq)?2Na2CO3•3H2O2(s)△H<0,如图是制取过碳酸钠 的示意图,步骤如下
过碳酸钠(2Na2CO3•3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂,易分解.可用纯碱与H2O2反应制取,反应方程式为:2Na2CO3(aq)+3H2O2(aq)?2Na2CO3•3H2O2(s)△H<0,如图是制取过碳酸钠 的示意图,步骤如下