题目内容
1.“保护环境,就是保护人类自己.”下列环境问题与其产生的主要原因不相符的是( )①“臭氧空洞”主要是大量使用氟氯代烃等引起的
②“光化学烟雾”主要是由NOx等引起的
③“赤潮”主要是由水体中P、N等元素过量引起的
④“白色污染”主要是由聚乙烯塑料等引起的
⑤“酸雨”主要是由空气中CO2浓度增大引起的
⑥“温室效应”主要是由空气中CO2浓度增大引起的.
| A. | 只有① | B. | 只有②③⑤ | C. | 只有⑤ | D. | 全部 |
分析 ①臭氧空洞主要与氟氯代烃等过量排放造成;
②光化学烟雾的形成主要是汽车尾气排放出的氮氧化物发生复杂的变化造成的;
③主要是水体富营养化导致水中的藻类生长繁殖过快所引起的;
④白色污染主要是由白色塑料等引起的;
⑤引起酸雨的主要气体是二氧化硫、二氧化氮等气体;
⑥造成温室效应的气体是二氧化碳.
解答 解:①“臭氧空洞”主要是大量使用氟氯代烃等引起的,故正确;
②“光化学烟雾”主要是由NO2等引起的,能引起人的呼吸道疾病,故正确;
③赤潮主要是由水体中P、N等元素过量引起的,造成水体富营养化,故正确;
④“白色污染”主要是由白色塑料等引起的,如聚乙烯、聚苯乙烯塑料,故正确;
⑤酸雨的主要形成原因是因为过度使用含硫化石燃料,SO2过度排放造成,故错误;
⑥“温室效应”主要是由空气中CO2浓度增大引起的,故正确;
故选C.
点评 本题主要考查了常见的环境污染,明确形成环境污染的原因,可以让学生了解形成实质,懂得保护环境,节约能源.

练习册系列答案
相关题目
12.甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景,现有如下实验:在体积为1L的密闭容器中,充入1mol CH3OH和1mol H2O,一定条件下发生反应:
CH3OH (g)+H2O (g)?CO2(g)+3H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示.
(1)已知:CH3OH(g)+$\frac{1}{2}$O2 (g)?CO2(g)+2H2 (g)△H1=-192.9kJ/mol K1
H2(g)+O2(g)?H2 O(g)△H2=-120.9kJ/mol K2
则甲醇与水蒸气催化重整反应的焓变△H3=-72.0kJ/mol.
(2)10~30 min内,氢气的平均反应速率v(H2)=0.06mol/(L•min).
(3)该反应的平衡常数表达式为K=$\frac{{K}_{1}}{{K}_{2}}$.
(4)下列措施中能使平衡时$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$)减小的是(双选)CD.
A.加入催化剂
B.恒容充入He(g),使体系压强增大
C.将H2(g)从体系中分离
D.再充入1molH2O.
CH3OH (g)+H2O (g)?CO2(g)+3H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示.
| 时间 物质 | 0 min | 10 min | 30 min | 60 min | 70 min |
| CO2(mol/L) | 0 | 0.2 | 0.6 | 0.8 | 0.8 |
| CH3OH(mol/L) | 1.0 | 0.8 | 0.4 | 0.2 | 0.2 |
H2(g)+O2(g)?H2 O(g)△H2=-120.9kJ/mol K2
则甲醇与水蒸气催化重整反应的焓变△H3=-72.0kJ/mol.
(2)10~30 min内,氢气的平均反应速率v(H2)=0.06mol/(L•min).
(3)该反应的平衡常数表达式为K=$\frac{{K}_{1}}{{K}_{2}}$.
(4)下列措施中能使平衡时$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$)减小的是(双选)CD.
A.加入催化剂
B.恒容充入He(g),使体系压强增大
C.将H2(g)从体系中分离
D.再充入1molH2O.
9.已知外电路中,电子由铜流向a极.有关如图所示装置的分析中,合理的一项是( )

| A. | 一段时间后Zn电极逐渐溶解 | |
| B. | 该装置中Cu极为正极,发生还原反应 | |
| C. | b极反应的电极反应式为:H2-2e-=2H+ | |
| D. | 电流方向:a电极→ →Cu电极 →Cu电极 |
7.在Na2O2与CO2的反应力,每生成5.6L O2(标况)时,转移电子数为( )
| A. | 2个 | B. | 0.25mol | C. | 3.01×1023个 | D. | 1mol |
 氨、硫、氯及其化合物对环境有着重要的影响,在化工生产和日常生活中的用途也十分广泛,如用做漂白剂、沉淀剂、农药、化肥等.
氨、硫、氯及其化合物对环境有着重要的影响,在化工生产和日常生活中的用途也十分广泛,如用做漂白剂、沉淀剂、农药、化肥等.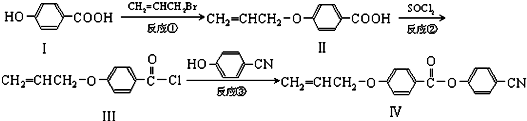
 .
. 也可与III发生类似反应③的反应,生成有机物V,V的结构简式是
也可与III发生类似反应③的反应,生成有机物V,V的结构简式是 .
.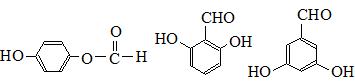 .
.
 .
. )有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
)有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )