题目内容
3.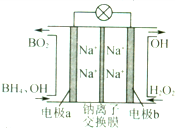 据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2做原料的燃料电池,负极材料采用Pt/C.正极材料采用MnO2,可用做空军通信卫星电源,其丁作原理如图所示.下列说法中错误的是( )
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2做原料的燃料电池,负极材料采用Pt/C.正极材料采用MnO2,可用做空军通信卫星电源,其丁作原理如图所示.下列说法中错误的是( )| A. | 电池放电时Na+从a极区移向b极区 | |
| B. | 电极b采用Mn O2,Mn O2既做电极材料又有催化作用 | |
| C. | 该电池的负极反应为BH${\;}_{4}^{-}$+8OH-一8e-═BO${\;}_{2}^{-}$+6H2O | |
| D. | 每消耗3molH2O2,转移的电子为3mol |
分析 以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,电解质溶液呈碱性,由工作原理装置图可知,负极发生氧化反应,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,正极H2O2发生还原反应,得到电子被还原生成OH-,电极反应式为H2O2+2e-=2OH-,结合原电池的工作原理和解答该题.
解答 解:A.原电池工作时,阳离子向正极移动,阴离子向负极移动,则Na+从a极区移向b极区,故A正确;
B.电极b采用MnO2为正极,H2O2发生还原反应,得到电子被还原生成OH-,MnO2既作电极材料又有催化作用,故B正确;
C.负极发生氧化反应生成BO2-,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,故C正确;
D.正极电极反应式为H2O2+2e-=2OH-,每消耗3molH2O2,转移的电子为6mol,故D错误;
故选D.
点评 本题考查原电池工作原理,涉及电极判断与电极反应式书写等问题,做题时注意从氧化还原的角度判断原电池的正负极以及电极方程式的书写,本题中难点和易错点为电极方程式的书写,注意化合价的变化.

练习册系列答案
相关题目
13.X、Y、Z、W为四种短周期主族元素.其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6.下列说法正确的是( )
| A. | Y、Z两元素的简单离子的半径Y>Z | |
| B. | Y元素最高价氧化物对应水化物的化学式为H2YO4 | |
| C. | 原子序数由小到大的顺序为W<X<Y<Z | |
| D. | X与W可以形成W2X、W2X2两种化合物 |
14.下列装置能形成原电池且灵敏电流计发生偏转的是( )
| A. | 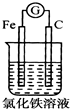 | B. | 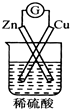 | C. |  | D. | 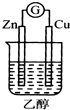 |
18. 如图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.已知放电时电池反应为:Pb+PbO2+4H++2SO42-═2PbSO4+2H2O.下列有关说法正确的是( )
如图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.已知放电时电池反应为:Pb+PbO2+4H++2SO42-═2PbSO4+2H2O.下列有关说法正确的是( )
 如图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.已知放电时电池反应为:Pb+PbO2+4H++2SO42-═2PbSO4+2H2O.下列有关说法正确的是( )
如图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.已知放电时电池反应为:Pb+PbO2+4H++2SO42-═2PbSO4+2H2O.下列有关说法正确的是( )| A. | K与N相接时,能量由电能转化为化学能 | |
| B. | K与N相接时,Pb上发生反应为:Pb-2e-═Pb2+ | |
| C. | K与M连接时,所用电源的a极为负极 | |
| D. | K与M连接时,PbO2上发生反应为:PbO2+4e_+4H++SO42-═PbSO4+2H2O |
8.若NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol过氧化钠与足量水反应转移2NA个电子 | |
| B. | 24克03和标准状况下11.2L氮气含有相同的分子数 | |
| C. | 1.8克重水(D2O)中所含质子数为NA | |
| D. | 100 mL 1.5mol/L氯化镁溶液中含0.15 mol Cl- |
12.下列离子方程式正确的是( )
| A. | 向沸水中滴加饱和的氯化铁溶液制取胶体:Fe3++3H2O═Fe(OH)3↓+3H+ | |
| B. | 碳酸氢镁溶液中加入足量的氢氧化钠溶液:Mg2++2HCO3-+2OH-═MgCO3↓+CO32-+2H2O | |
| C. | 硝酸铝溶液中加入过量的氨水:Al3++4NH3+2H2O═AlO2-+4NH4+ | |
| D. | 淀粉碘化钾试纸在潮湿空气中变蓝:4I-+O2+2H2O═2I2+4OH- |
20.NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 等物质的量的N2和CO所含分子数均为NA | |
| B. | 1.7gH2O2中含有的电子数为0.9NA | |
| C. | 10mL质量分数98%的H2SO4,用水稀释至100mL,H2SO4的质量分数为9.8% | |
| D. | 1molCl2与足量的铁反应,转移的电子数为3NA |
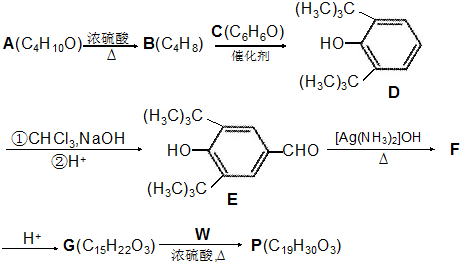
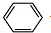 +R2C$\stackrel{催化剂}{→}$
+R2C$\stackrel{催化剂}{→}$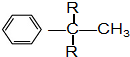 (R为烷基)
(R为烷基)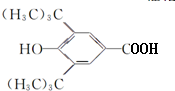 ;E中含有的官能团名称是羟基和醛基;
;E中含有的官能团名称是羟基和醛基;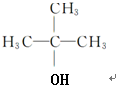 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O;该反应类型为消去反应;
+H2O;该反应类型为消去反应; +H2O;该反应类型为酯化反应;
+H2O;该反应类型为酯化反应; ,C的化学式为Mg(OH)2
,C的化学式为Mg(OH)2