题目内容
11.合成P(一种抗氧剂)的路线如图: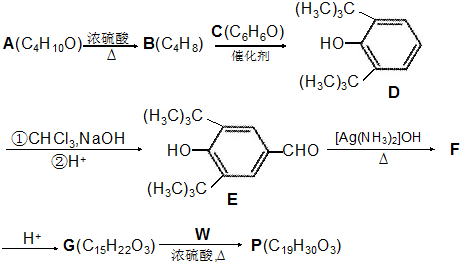
已知:①
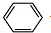 +R2C$\stackrel{催化剂}{→}$
+R2C$\stackrel{催化剂}{→}$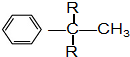 (R为烷基)
(R为烷基)②A和W互为同分异构体,A分子中有两种不同化学环境的氢原子,W核磁共振氢谱显示5组峰,且峰面积比为3:2:2:2:1.
(1)G的结构简式是
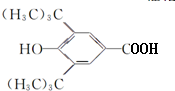 ;E中含有的官能团名称是羟基和醛基;
;E中含有的官能团名称是羟基和醛基;(2)A→B的化学方程式是
 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O;该反应类型为消去反应;
+H2O;该反应类型为消去反应;(3)B经催化加氢生成的物质的名称是2-甲基丙烷;
(4)G和W反应生成P的化学方程式是
 +CH3CH2CH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$
+CH3CH2CH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$ +H2O;该反应类型为酯化反应;
+H2O;该反应类型为酯化反应;(5)关于C和P,下列说法正确的是①③⑤⑥.
①C和P都能使FeCl3溶液显色;②C和P都能与浓溴水反应并生成白色沉淀;③C和P都能与Na2CO3溶液反应;④C和P含有的官能团种类相同;⑤P能发生水解反应而C不能; ⑥等量的C和P与NaOH溶液反应时最多消耗NaOH的量不相同.
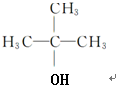
分析 A在加热浓硫酸作用下反应生成B,A和B的化学式相差一个H2O,则发生了消去反应,所以A是醇,B是烯烃,根据C的分子式和D的结构简式可知,C为苯酚,B和苯酚反应生成 ,所以B是
,所以B是 ,A分子中有两种不同化学环境的氢原子,所以A的结构简式为:
,A分子中有两种不同化学环境的氢原子,所以A的结构简式为: ,
, 反应生成
反应生成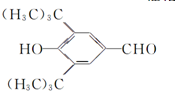 ,
, 和银氨溶液反应生成F,F的结构简式为:
和银氨溶液反应生成F,F的结构简式为: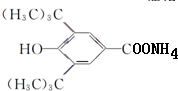 ,酸性条件下,F反应生成G为
,酸性条件下,F反应生成G为 ,A和W互为同分异构体,W核磁共振氢谱显示5组峰,且峰面积比为3:2:2:2:1,W的结构简式为:CH3CH2CH2CH2OH,G和W发生酯化反应生成P,P的结构简式为:
,A和W互为同分异构体,W核磁共振氢谱显示5组峰,且峰面积比为3:2:2:2:1,W的结构简式为:CH3CH2CH2CH2OH,G和W发生酯化反应生成P,P的结构简式为: ,据此答题.
,据此答题.
解答 解:A在加热浓硫酸作用下反应生成B,A和B的化学式相差一个H2O,则发生了消去反应,所以A是醇,B是烯烃,根据C的分子式和D的结构简式可知,C为苯酚,B和苯酚反应生成 ,所以B是
,所以B是 ,A分子中有两种不同化学环境的氢原子,所以A的结构简式为:
,A分子中有两种不同化学环境的氢原子,所以A的结构简式为: ,
, 反应生成
反应生成 ,
, 和银氨溶液反应生成F,F的结构简式为:
和银氨溶液反应生成F,F的结构简式为: ,酸性条件下,F反应生成G为
,酸性条件下,F反应生成G为 ,A和W互为同分异构体,W核磁共振氢谱显示5组峰,且峰面积比为3:2:2:2:1,W的结构简式为:CH3CH2CH2CH2OH,G和W发生酯化反应生成P,P的结构简式为:
,A和W互为同分异构体,W核磁共振氢谱显示5组峰,且峰面积比为3:2:2:2:1,W的结构简式为:CH3CH2CH2CH2OH,G和W发生酯化反应生成P,P的结构简式为: ,
,
(1)根据上面的分析,G为 ,E为
,E为 ,E中含有的官能团名称是羟基和醛基,
,E中含有的官能团名称是羟基和醛基,
故答案为: ;羟基和醛基;
;羟基和醛基;
(2)A→B的化学方程式是为 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O,该反应类型为消去反应,
+H2O,该反应类型为消去反应,
故答案为: $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O;消去反应;
+H2O;消去反应;
(3)B是 ,B经催化加氢生成的物质是CH3CH(CH3)2,名称是2-甲基丙烷,
,B经催化加氢生成的物质是CH3CH(CH3)2,名称是2-甲基丙烷,
故答案为:2-甲基丙烷;
(4)G和W反应生成P的化学方程式是 +CH3CH2CH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$
+CH3CH2CH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$ +H2O,该反应类型为酯化反应,
+H2O,该反应类型为酯化反应,
故答案为: +CH3CH2CH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$
+CH3CH2CH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$ +H2O;酯化反应;
+H2O;酯化反应;
(5)①C和P中都有酚羟基,所以都能使FeCl3溶液显色,故正确;
②P不都能与浓溴水发生邻对位取代反应,故错误;
③C和P中都有酚羟基,所以C和P都能与Na2CO3溶液反应生成碳酸氢钠,故正确;
④P中含有酯基,而C中没有,故错误;
⑤P中含有酯基,能发生水解反应而C不能,故正确;
⑥每摩尔C最多消耗NaOH1mol,每摩尔P最多消耗NaOH2mol,故正确,
故选①③⑤⑥.
点评 本题考查了有机物的推断,明确物质含有的官能团及其性质是解本题的关键,结合题给信息进行分析解答,难度中等.

| A. | KNO3 | B. | CO(NH2)2 | C. | Ca(H2PO4)2 | D. | (NH4)2SO4 |
| A. | 硝酸保存在带橡胶塞的棕色细口瓶中,置于冷暗处 | |
| B. | 用瓷坩埚来加热烧碱或纯碱使其熔化 | |
| C. | 用蒸馏水鉴别溴蒸气和二氧化氮气体 | |
| D. | 用盐酸为抛光液,抛光单晶硅 |
| A. | CO2、NO2、SO2属于大气污染物 | |
| B. | 利用60Co的放射性可治疗某些疾病,60Co和59Co互为同位素 | |
| C. | 大气中CO2含量的增加会导致温室效应加剧 | |
| D. | 食盐可作调味剂,也可作食品防腐剂 |
| A. | 室温下,0.1 mol/LW的气态氢化物的水溶液的pH>1 | |
| B. | Z的最高价氧化物能与水反应生成相应的酸 | |
| C. | Y单质在一定条件下可以与氧化铁发生置换反应 | |
| D. | 原子半径由小到大的顺序:X<Y<Z<W |
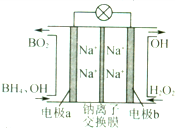 据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2做原料的燃料电池,负极材料采用Pt/C.正极材料采用MnO2,可用做空军通信卫星电源,其丁作原理如图所示.下列说法中错误的是( )
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2做原料的燃料电池,负极材料采用Pt/C.正极材料采用MnO2,可用做空军通信卫星电源,其丁作原理如图所示.下列说法中错误的是( )| A. | 电池放电时Na+从a极区移向b极区 | |
| B. | 电极b采用Mn O2,Mn O2既做电极材料又有催化作用 | |
| C. | 该电池的负极反应为BH${\;}_{4}^{-}$+8OH-一8e-═BO${\;}_{2}^{-}$+6H2O | |
| D. | 每消耗3molH2O2,转移的电子为3mol |

下列说法正确的是( )
| A. | 滤液A中的阳离子为Fe2+、Fe3+、H+ | B. | 样品中Fe元素的质量为2.24 g | ||
| C. | 样品中CuO的质量为4.0 g | D. | V=896 mL |
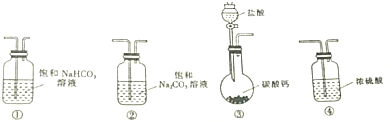
(1)选取必要的实验装置,正确的连接顺序为③①②(填序号)
(2)为确定制得的固体样品是纯净的NaHCO3,小组同学提出下列实验方案
甲方案:将样品溶液与饱和澄清石灰水反应,观察现象
乙方案:将样品溶液与BaCl4,观察现象
丙方案:测得pH法
丁方案:热重分析法
①判定甲方案不可行(填“可行”或“不可行”)
②为判断乙方案的可行性,某同学用分析纯的NaHCO3配制的溶液,与BaCl4溶液等体积混合进行实验,结果如下.
| NaHCO3溶液 BaCl3浓度 | 0.2mol•L-1 | 0.1mol•L-1 | 0.02mol•L-1 |
| 0.2mol•L-1 | 浑浊 | 浑浊 | 少许浑浊 |
| 0.1mol•L-1 | 浑浊 | 少许浑浊 | 无现象 |
| 0.02mol•L-1 | 少许浑浊 | 无现象 | 无现象 |
[已知0.1mol•L-1NaHCO3溶液电离出的c(CO32-)为0.0011mol•L-1,Ksp(BaCO3)=5.1×10-9]
②产生浑浊的离子方程式为Ba2++2HCO3-=BaCO3↓+CO2↑+H2O.
③使用pH计进行测定的丙方案是取等质量的固体样品和分析纯NaHC03样品分别溶解于等量的水中,分别用pH计测pH.
(3)某溶液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中$\frac{c({I}^{-})}{c(C{l}^{-})}$为:4.8×10-7,已知Ksp(AgCl)=1.8×10-10,Ksp(Agl)=8.5×10-17.
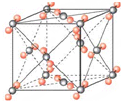 干冰晶胞如图所示,边长a=5.72×10-8cm,该温度下干冰的密度为1.56g/cm3
干冰晶胞如图所示,边长a=5.72×10-8cm,该温度下干冰的密度为1.56g/cm3