��Ŀ����
20�� ijѧϰС��̽��NaHCO3��Na2HCO3�����ᣨ����Ũ�Ⱦ�Ϊ1mol��L-1����Ӧ�����е���ЧӦ��ʵ�����������ݣ�
ijѧϰС��̽��NaHCO3��Na2HCO3�����ᣨ����Ũ�Ⱦ�Ϊ1mol��L-1����Ӧ�����е���ЧӦ��ʵ�����������ݣ�| ��� | 35mL�Լ� | ���� | ����¶�ǰ/�� | ����¶Ⱥ�/�� |
| �� | ˮ | 2.5gNaHCO3 | 20.0 | 18.5 |
| �� | ˮ | 3.2gNa2CO3 | 20.0 | 24.3 |
| �� | ���� | 2.5gNaHCO3 | 20.0 | 16.2 |
| �� | ���� | 3.2gNa2CO3 | 20.0 | 25.1 |
��1��д��NaHCO3�����ᷢ����Ӧ�����ӷ���ʽHCO3-+H+=CO2��+H2O
��2��������ʵ��ó��Ľ����ǣ�Na2CO3��Һ������ķ�Ӧ�Ƿ��ȣ�����ȡ����ȡ���ͬ����Ӧ��NaHCO3��Һ�����ᷴӦ�����ȷ�Ӧ
��3������ͼ�л���Na2CO3�����ᷴӦǰ�������仯���ߣ���ע����Ӧ�����������͡�����������������
���� ��1��̼�����������ᷴӦ�����Ȼ��ơ�������̼�����ˮ���ݴ�д����Ӧ�����ӷ���ʽ��
��2������ʵ��٢ۿ�֪��̼������������ķ�ӦΪ���ȷ�Ӧ������ʵ��ڢܿ�֪��̼����������ķ�ӦΪ���ȷ�Ӧ��
��3��̼����������ķ�ӦΪ���ȷ�Ӧ����Ӧ���������������������������ݴ˻�����Ӧǰ�������仯���ߣ�
��� �⣺��1��̼�����������ᷴӦ��ʵ��Ϊ��̼����������������ӷ�Ӧ���ɶ�����̼�����ˮ����Ӧ�����ӷ���ʽΪ��HCO3-+H+=CO2��+H2O��
�ʴ�Ϊ��HCO3-+H+=CO2��+H2O��
��2������ʵ��ٿ�֪��̼����������ˮ����Һ�¶ȴ�20�潵�͵�18.5�棬��ʵ�����̼�����������ᷴӦ����Һ�¶ȴ�20�潵��16.2�棼18.5�棬ͨ����Ӧ�����Һ�¶ȸ��ͣ�֤����Ӧ��Ϊ���ȷ�Ӧ��
ͬ��������ʵ���̼��������ˮ�����Һ�¶ȴ�20�����ߵ�24.3�棬ʵ�����̼���������ᷴӦ���¶ȴ�20�����ߵ�25.1�棾24.3�棬̼���������ᷴӦ����Һ���¶ȱ�̼��������ˮ�����ߵ��¶ȸ��ߣ�֤��̼����������ķ�ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ�����ȣ����ȣ�
��3�����ݣ�2���ķ�����֪��̼����������ķ�ӦΪ���ȷ�Ӧ��˵����Ӧ�����������������������ߣ��ݴ˿ɻ����ķ�Ӧǰ�������仯����Ϊ��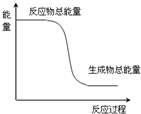 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���� ���⿼����̽�����ȷ�Ӧ�����ȷ�Ӧ�ķ�������Ŀ�Ѷ��еȣ�ע�����ջ�ѧ��Ӧ�е������仯����ȷ̽�����ȷ�Ӧ�����ȷ�Ӧ�ķ���������������ѧ���ķ���������������������������

| A�� | �⻯��ķе㣺Zһ������Y | |
| B�� | ����������Ӧˮ��������ԣ�Xǿ��Y | |
| C�� | W��X��Y��Z���ֱܷ�����Ԫ���γɹ��ۻ����� | |
| D�� | ����W��Y��Z����Ԫ����ɵĻ����ﲻ������������ |
��1��250��ʱ�������Ͻ�Ϊ��������4L������ͨ��6mol CO2��6mol CH4���������·�Ӧ��
CO2 ��g��+CH4��g��?2CO��g��+2H2��g����ƽ����ϵ�и��������������±���
| ���� | CH4 | CO2 | CO | H2 |
| ������� | 0.1 | 0.1 | 0.4 | 0.4 |
����֪��CH4��g��+2O2��g��=CO2��g��+2H2O��g����H=-890.3kJ•mol-1
CO��g��+H2O ��g��=CO2��g��+H2 ��g����H=+2.8kJ•mol-1
2CO��g��+O2��g��=2CO2��g����H=-566.0kJ•mol-1
��ӦCO2��g��+CH4��g��?2CO��g��+2H2��g�� �ġ�H=+247.3 kJ•mol-1
��2���Զ������ѱ��渲��Cu2Al2O4Ϊ���������Խ�CO2��CH4ֱ��ת�������ᣮ
���ڲ�ͬ�¶��´����Ĵ�Ч�������������������ͼ1��ʾ��250��300��ʱ���¶����߶�������������ʽ��͵�ԭ�����¶ȳ���250��ʱ�������Ĵ�Ч�ʽ���
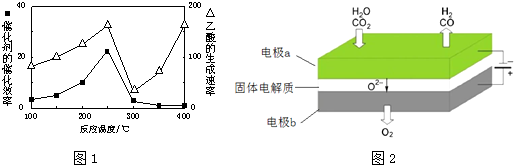
��Ϊ����߸÷�Ӧ��CH4��ת���ʣ����Բ�ȡ�Ĵ�ʩ�����������Сѹǿ������CO2��Ũ��
�۽�Cu2Al2O4�ܽ���ϡ�����е����ӷ���ʽΪ3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO��+16H2O
��3��Li2O��Na2O��MgO��������CO2�������Ѱ������CO2���������ʣ����н����������ab
a�����ڼ�����������Ѱ��
b�����ڢ�A����A��Ԫ���γɵ���������Ѱ��
c�����ھ���ǿ�����Ե�������Ѱ��
��4�����÷�ӦA�ɽ��ͷŵ�CO2ת��Ϊ���й�ҵ���ü�ֵ�IJ�Ʒ��
��ӦA��CO2+H2O$\frac{\underline{\;���\;}}{����}$CO+H2+O2���µ�⼼���ܸ�Чʵ�ַ�ӦA������ԭ��ʾ��ͼ2���£�CO2�ڵ缫a�ŵ�ķ�Ӧʽ��CO2+2e-�TCO+O2-��
��֪��N2��g��+O2��g��=2NO��g����H=+180.5kJ/mol
N2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol
2H2��g��+O2��g��=2H2O��g����H=-483.6kJ/mol
д������������������һ�����������ˮ�������Ȼ�ѧ����ʽ��4NH3��g��+5O2��g���T4NO��g��+6H2O��g����H=-905.0kJ/mol��
��2�������ܱ������н��еĺϳɰ���Ӧ���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
| t/K | 298 | 398 | 498 | �� |
| K | 4.1��106 | K1 | K2 | �� |
���ϱ���K1��K2�����������=����������
��3������ϳ����г���10molN2��40molH2���а��ĺϳɣ�ͼA��ͼBΪһ���¶���ƽ�������а��������������ѹǿ��p���Ĺ�ϵͼ�� ��
������˵����ȷ����ABD������ţ���
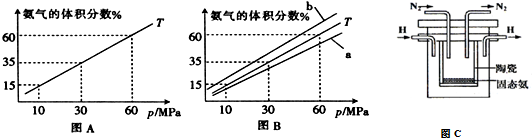
A��ͼ�����߱���������ϵѹǿ��p������������߰����ڻ���������������
B�����ͼB��T=500�棬���¶�Ϊ450��ʱ��Ӧ��������b
C����ҵ�ϲ���500���¶ȿ���Ч��߷�Ӧ���ʺ͵�����ת����
D���� 2v����H2��=3v����NH3��ʱ����Ӧ�ﵽƽ��״̬
E�������ڻ�������ܶȱ��ֲ���ʱ����Ӧ�ﵽƽ��״̬
��ͼA�а������������Ϊ15%ʱ��N2��ת����Ϊ32.61%��
��4����1998��ϣ������˹��´�ѧ��Marmellos��Stoukides���ø����ӵ����Ե�SCY�մɣ��ܴ���H+����ʵ���˸��³�ѹ�¸�ת���ʵĵ绯ѧ�ϳɰ�����ʵ��װ����ͼC���������ĵ缫��ӦʽN2+6e-+6H+=2NH3��
��5��25��ʱ��Ksp[Mg��OH��2]=5.61��10-12��Ksp[MgF2]=7.42��10-11������˵����ȷ����BD��
A��25��ʱ������Mg��OH��2��Һ��c��OH-�����ڱ���MgF2��Һ��c��F-��
B��25��ʱ��ij����Mg��OH��2��Һ��c��Mg2+��=0.0561 mol•L-1������Һ��pH=9
C�� 25��ʱ����Mg��OH��2������Һ�м���������NH4Cl���壬��Һ����壬Ksp[Mg��OH��2]����
D��25��ʱ����Mg��OH��2����Һ�м���NaF��Һ��Mg��OH��2����ת��ΪMgF2��
| A�� | Cl2 | B�� | HCl | C�� | HClO | D�� | H2O |
| A�� | ����ڷ�������Ҫ��ӦΪ��2Fe2++H2O2+2H+=2Fe3++2H2O | |
| B�� | ����ڿ�����ˮ�������ǿ����������H2O2 | |
| C�� | ������� CuCO3����CuOҲ�ɵ�����Һ��pH | |
| D�� | ����ݵIJ���Ϊ����©���м��������������ˮ����û���壬��ˮ��Ȼ���£��ظ����� 2��3�� |
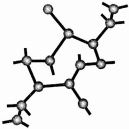 ��������һ���������ǽ������ϣ���Ҫ�Ц�-������ͦ�-���������־��ͣ����Ƕ�����[SiN4]�������干�ö���ԭ�ӹ��ɵ���ά�ռ�����ṹ����-������Ľṹ��ͼ��ʾ��
��������һ���������ǽ������ϣ���Ҫ�Ц�-������ͦ�-���������־��ͣ����Ƕ�����[SiN4]�������干�ö���ԭ�ӹ��ɵ���ά�ռ�����ṹ����-������Ľṹ��ͼ��ʾ�� ����ȥ����ԭ�Ӻ��ʣ�ಿ�ּ�Si44-��ԭ�������Ϊ����������ṹ�������ϵ�4����ԭ�ӳ�������������3������������˴���3�������������γ����ӵĻ�ѧʽΪSi3O96-��n������������˴���4���������Ӻ��γɵ����ʵĻ�ѧʽ��SiO2��
����ȥ����ԭ�Ӻ��ʣ�ಿ�ּ�Si44-��ԭ�������Ϊ����������ṹ�������ϵ�4����ԭ�ӳ�������������3������������˴���3�������������γ����ӵĻ�ѧʽΪSi3O96-��n������������˴���4���������Ӻ��γɵ����ʵĻ�ѧʽ��SiO2��
 ����MnO2���乤��ԭ����ͼ����ʾ����طŵ�ʱNa+��a����д��a����b������ͬ����������b�������õ�صĸ�����ӦʽΪBH4-+8OH--8e-=BO2-+6H2O��
����MnO2���乤��ԭ����ͼ����ʾ����طŵ�ʱNa+��a����д��a����b������ͬ����������b�������õ�صĸ�����ӦʽΪBH4-+8OH--8e-=BO2-+6H2O��