题目内容
将69 g NO2(含少量N2O4)通入水中,关于此过程下列说法正确的是(NA表示阿伏加德罗常数)
| A.69 g NO2与N2O4混合气体所含原子数介于4.5 NA至9.0 NA之间 |
| B.此反应中转移的电子数为NA |
| C.最终可收集到11.2 L无色气体 |
| D.若将所得硝酸制成浓硝酸,常温下最多可溶解0.25 mol铁。 |
B
解析试题分析:69 g NO2是1.5mol,其混合气体所含原子数是定值,是4.5 NA,A错误;与水反应时产物中有2/3的氮化合变成了+5价,故此反应中转移的电子数为NA,B正确。C中没有说明是标准状况无法判断,错误。若将所得硝酸制成浓硝酸即为1mol,产物中只有二氧化氮生成,根据电子守恒,铁化合价变成正三价,常温下最多可溶解1/3 mol铁,错误;
考点:本题考查氧化还原原理的运用。

 金钥匙试卷系列答案
金钥匙试卷系列答案常温下,某200mL稀硫酸和稀硝酸的混合溶液最多能溶解 19.2g铜粉(已知硝酸只被还原为NO气体),若再取等体积的该混合酸向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列有关分析错误的是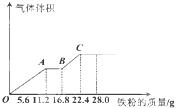
| A.原混合酸中NO3—的物质的量为0.2 mol |
| B.原混合酸中H2SO4物质的量浓度为2 mol/L |
| C.取25mL原混合酸加水稀释至1 L后溶液的pH =1 |
| D.OA段与BC段反应中电子转移的物质的量之比为3:1 |
下列实验现象与氧化还原反应有关的是
| A.SO2通入品红溶液中,溶液褪色 |
| B.新制氯水密闭放置一段时间后浅黄绿色消失 |
| C.向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀 |
| D.向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成 |
12月2日1时30分,“嫦娥三号”奔月探测器发射成功。“嫦娥三号”装有电解水制氢气装置,以提供气象探测系统所需要的高纯度氢气。围绕反应方程式2H2O 2H2↑+O2↑,下列有关判断正确的是
2H2↑+O2↑,下列有关判断正确的是
| A.氧化剂是氢元素 |
| B.还原产物是O2 |
| C.H2O既有氧化性也有还原性 |
| D.2molH2O反应,转移了8mol电子 |
实验室可以用高锰酸钾与浓盐酸反应制取氯气,反应的化学方程式如下:2KMn04+16HCl(浓) = 2KCl+5Cl2↑+2MnCl2+8H20
对于该反应,下列说法正确的是
| A.HCl是氧化剂 | B.是非氧化还原反应 |
| C.反应中锰元素被还原 | D.反应中氢元素的化合价升高 |
下列变化,需要加入还原剂才能实现的是
| A.FeCl2→FeCl3 | B.CO2→C | C.NaAlO2→AlCl3 | D.HCl→Cl2 |
为了测定某铜银合金成分,将30 g合金完全溶于80 mL 13.5 mol/L的浓硝酸中,待反应完全后,收集到0.3 mol气体,并测得溶液中c(H+)是1 mol/L。假设反应后溶液体积仍为80 mL,则合金中银的质量分数为
| A.36% | B.66.3% | C.78.7% | D.96.6% |
著名化学家徐光宪获得国家最高科学技术奖,以表彰他在稀土萃取理论方面作出的贡献。已知:金属铈(稀土元素)在空气中易氧化变暗,受热时燃烧,遇水很快反应。(注:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+>I2。)下列说法正确的是
A.铈溶于氢碘酸的化学方程式可表示为:Ce + 4HI  CeI4 + 2H2↑ CeI4 + 2H2↑ |
| B.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4+ + 2Fe2+ = Ce3+ + 2Fe3+ |
| C.在一定条件下,电解熔融状态的CeO2制Ce,在阴极获得铈 |
| D.铈的四种核素13658Ce、13858Ce、14058Ce、14258Ce,它们互称为同素异形体 |
已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O,其中1mol氧化剂在反应中得到的电子为
| A.10mol | B.11mol | C.12mol | D.13mol |