题目内容
常温下,某200mL稀硫酸和稀硝酸的混合溶液最多能溶解 19.2g铜粉(已知硝酸只被还原为NO气体),若再取等体积的该混合酸向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列有关分析错误的是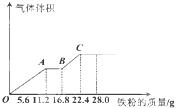
| A.原混合酸中NO3—的物质的量为0.2 mol |
| B.原混合酸中H2SO4物质的量浓度为2 mol/L |
| C.取25mL原混合酸加水稀释至1 L后溶液的pH =1 |
| D.OA段与BC段反应中电子转移的物质的量之比为3:1 |
C
解析试题分析:A、铜粉最多能溶解19.2克,是0.3mol,失去0.6 mol电子,说明含硝酸根离子0.2 mol,考虑生成硫酸铜,则至少有硝酸0.2 mol,硫酸0.3 mol;铁粉则最多能溶解22.4g,是0.4 mol,失去0.8 mol电子.说明还有0.1 mol硫酸反应生成硫酸亚铁和氢气,则有0.2 mol硝酸和0.4 mol硫酸亚铁。因此,原混合酸中NO3-的物质的量为0.2mol,硝酸浓度是1 mol /L,正确;B、同理可知:硫酸的物质的量为0.4mol,硫酸浓度是2mol/L, B正确;C、原混合酸中C(H+)=5mol/L,稀释50倍后,C(H+)="0.1" mol/L,pH=1,正确;D、由AB段气体数量不变可知,此阶段是Fe3+与单质铁之间的反应,BC阶段发生的是H+与单质铁的反应,OA段消耗0.2mol铁且此阶段反应结束时,溶液中还剩余有H+,说明此时溶液中NO3-全部反应完了,OA段电子转移的物质的量为0.6mol,BC阶电子转移的物质的量为0.2mol,两者的物质的量之比为3:1,错误。
考点:本题考查硝酸的性质及计算、图像的分析。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应类型属于阴影部分的是
| A.2Na2O2+2H2O=4NaOH+O2↑ |
B.NH4HCO3 NH3↑+CO2↑+H2O NH3↑+CO2↑+H2O |
| C.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| D.Br2+2KI=I2+2KBr |
制取下列物质一定有氧化还原反应发生的是
| A.NH3 | B.Mg | C.FeCl3 | D.NaAlO2 |
将69 g NO2(含少量N2O4)通入水中,关于此过程下列说法正确的是(NA表示阿伏加德罗常数)
| A.69 g NO2与N2O4混合气体所含原子数介于4.5 NA至9.0 NA之间 |
| B.此反应中转移的电子数为NA |
| C.最终可收集到11.2 L无色气体 |
| D.若将所得硝酸制成浓硝酸,常温下最多可溶解0.25 mol铁。 |
工业上可用硫酸铝与硫黄焙烧制备氧化铝:2Al2(SO4)3+3S  2Al2O3+9SO2↑,下列有关说法中正确的是( )
2Al2O3+9SO2↑,下列有关说法中正确的是( )
| A.反应中Al2(SO4)3被氧化 |
| B.Al2(SO4)3、Al2O3均含有离子键和共价键 |
| C.5.1 g Al2O3含有9.03×1022个阴离子 |
| D.该反应中,每转移0.3 mol电子生成5.04 L SO2 |
在下列变化中,需要加入合适的氧化剂才能实现的是( )
| A.HCl→H2 | B.CO2→CO | C.Fe2O3→Fe | D.Br-→Br2 |
将18 g铜和铁的混合物投入200 mL稀硝酸中,充分反应后得到标准状况下2.24 L NO,剩余9.6 g金属;继续加入200 mL等浓度的稀硝酸,金属完全溶解,又得到标准状况下2.24 L NO。若向反应后的溶液中加入KSCN溶液,溶液不变红,则下列说法中正确的是( )
| A.原混合物中铜和铁各0.15 mol |
| B.稀硝酸的物质的量浓度为1 mol·L-1 |
| C.第一次剩余9.6 g金属为铜和铁 |
| D.再加入上述200 mL稀硝酸,还会得到标准状况下2.24 L NO |
某化学兴趣小组在奥运五连环中填入了5种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型和属于氧化还原反应的个数有( )
| A.复分解反应、1个 | B.分解反应、2个 |
| C.化合反应、3个 | D.置换反应、2个 |
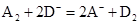 ,则氧化性:A2 > D2
,则氧化性:A2 > D2