题目内容
为了测定某铜银合金成分,将30 g合金完全溶于80 mL 13.5 mol/L的浓硝酸中,待反应完全后,收集到0.3 mol气体,并测得溶液中c(H+)是1 mol/L。假设反应后溶液体积仍为80 mL,则合金中银的质量分数为
| A.36% | B.66.3% | C.78.7% | D.96.6% |
A
解析试题分析由于HNO3的还原产物为NO或NO2或二者的混合物,根据N原子守恒:则被还原的HNO3的物质的量等于气体的物质的量:n(HNO3)="=0.3" mol,设合金中银的质量为x,则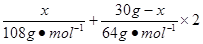 =13.5mol·L-1×0.08L-1mol·L-1×0.08L-0.3mol,x="10.8" g
=13.5mol·L-1×0.08L-1mol·L-1×0.08L-0.3mol,x="10.8" g
银的质量分数:w(Ag)=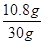 ×100%=36%。
×100%=36%。
考点:本题考查元素守恒法进行计算。

练习册系列答案
相关题目
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应类型属于阴影部分的是
| A.2Na2O2+2H2O=4NaOH+O2↑ |
B.NH4HCO3 NH3↑+CO2↑+H2O NH3↑+CO2↑+H2O |
| C.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| D.Br2+2KI=I2+2KBr |
下列四种基本类型反应中一定属于氧化还原反应的是( )
| A.复分解反应 | B.分解反应 | C.化合反应 | D.置换反应 |
将69 g NO2(含少量N2O4)通入水中,关于此过程下列说法正确的是(NA表示阿伏加德罗常数)
| A.69 g NO2与N2O4混合气体所含原子数介于4.5 NA至9.0 NA之间 |
| B.此反应中转移的电子数为NA |
| C.最终可收集到11.2 L无色气体 |
| D.若将所得硝酸制成浓硝酸,常温下最多可溶解0.25 mol铁。 |
下列属于右边关系图中阴影部分的化学反应是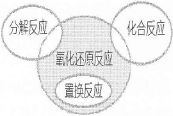
A.2Na+O2 Na2O2 Na2O2 |
| B.2Na2O2+2CO2=2Na2CO3+O2 |
C.2KMnO4 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
| D.Fe+H2SO4=FeSO4+H2↑ |
对剧毒的氰化物可在碱性条件下用如下方法进行处理:2CN-+8OH-+5Cl2=2CO2+N2+10Cl-+4H2O。下列判断正确的是
| A.当有0.2mol CO2生成时,溶液中阴离子的物质的量增加1mol |
| B.该反应中,每有2molCN-反应,转移电子为10mol |
| C.上述反应中的还原剂是OH- |
| D.还原性:C1->CN- |
对于反应14CuSO4+5FeS2+12H2O→7Cu2S+5FeSO4+12H2SO4,下列说法正确的是( )
| A.只有硫酸铜作氧化剂 |
| B.SO42-既不是氧化产物又不是还原产物 |
| C.被氧化的硫与被还原的硫的质量比为3:7 |
| D.1mol硫酸铜可以氧化5/7mol的硫原子 |
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如下图所示。有关说法不正确的是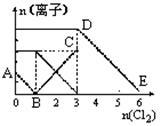
| A.线段BC代表Fe3+物质的量的变化情况 |
| B.原混合溶液中n(FeBr2)=3mol |
| C.当通入Cl22mol时,溶液中已发生的离子反应可表示为: 2Fe2++2I-+2C12=2Fe3++I2+4Cl- |
| D.原溶液中n(Fe2+):n(I-):n(Br-)=3:1: 2 |
反应①、②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是
| A.两个反应中均为硫元素被氧化 |
| B.碘元素在反应①中被还原,在反应②中被氧化 |
| C.氧化性:MnO2>SO42->IO3->I2 |
| D.反应①、②中生成等量的I2时转移电子数比为1:5 |