题目内容
4.高炉炼铁中发生的基本反应如下:FeO(s)+CO(g)?Fe (s)+CO2(g)已知1100℃,K=0.263
(1)1100℃时,若反应向正向进行,高炉内CO2和CO的体积比值逐渐增大直至不变.(填“增大”“减小”或“不变”)
(2)1100℃时,测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下该反应是否处于平衡状态否(填“是”或“否”),此时化学反应速率是V正大于V逆(填“大于”、“小于”或“等于”),其原因是浓度商Q=$\frac{0.025mol/L}{0.1mol/L}$=0.25<K=0.263,说明平衡正向进行.
分析 (1)反应是吸热反应,升温平衡正向进行,最后达到新的化学平衡;
(2)依据浓度计算浓度商结合平衡常数进行比较判断反应进行的方向.
解答 解:(1)FeO(固)+CO(气)?Fe(固)+CO2(气)△H>0,已知1100℃时K=0.263.反应是吸热反应,温度升高,化学平衡正向移动后达到新的平衡,高炉内CO2和CO的体积比值会增大,最后达到平衡状态,体积比不变,
故答案为:增大;不变;
(3)1100℃时测得高炉中c(CO2)=0.025mol•L-1,c(CO)=0.1mol•L-1,浓度商Q=$\frac{0.025mol/L}{0.1mol/L}$=0.25<K=0.263,说明平衡正向进行,反应未达到平衡,v正>v逆;
故答案为:否;大于;浓度商Q=$\frac{0.025mol/L}{0.1mol/L}$=0.25<K=0.263,说明平衡正向进行.
点评 本题考查了化学平衡、平衡常数影响因素分析判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
15.2.0LAlCl3溶液中含Cl-9.03×1023个,则溶液物质的量浓度是( )
| A. | 0.1mol/L | B. | 0.25mol/L | C. | 1mol/L | D. | 1.5mol/L |
15.在一固定容积为2L的密闭容器中加入4mol的N2和12mol的H2,在一定条件下发生反应:
N2(g)+3H2(g)?2NH3(g)△H<0
(1)若在5min时反应达到平衡,此时测得NH3的物质的量为4mol.则前5min的平均反应速率v(N2)=0.2mol/(L•min).平衡时H2的转化率为50%.该温度下的平衡常数K1=$\frac{4}{27}$(用分数表示);若反应开始时,将1molN2和3molH2通入到该容器,再达新平衡时的平衡常数为K2,则K2=K1(填“>”、“<”或“=”)
(2)平衡后,若要提高H2的转化率,可以采取的措施有C.
A.加了催化剂B.充入一定量的Ne
C.降低反应体系的温度D.再充入2mol的Ne和6mol的H2
(3)其化学平衡常数K与温度T的关系如表所示:
请完成下列问题:
①试比较K1、K2的大小,K1>K2(填“>”、“<”或“=”).
②400℃时,反应2NH3(g)?N2(g)+3H2(g)的化学平衡常数为2,2L的容器中,当测得NH3、N2和H2物质的量分别为6mol、4mol和2mol时,则该反应的v(N2)减>v(N2)增(填“>”、“<”或“=”).
(4)根据化学反应速率和化学平衡理论,联合合成氨的生产实际,你认为下列说法不正确的是C
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.勒夏特列原理可指导怎样使用有限原料多出产品
C.催化剂的使用是提高产品产率的有效方法
D.正确利用化学反应速率和化学反应限度理论都可以提高化工生产的综合经济效益.
N2(g)+3H2(g)?2NH3(g)△H<0
(1)若在5min时反应达到平衡,此时测得NH3的物质的量为4mol.则前5min的平均反应速率v(N2)=0.2mol/(L•min).平衡时H2的转化率为50%.该温度下的平衡常数K1=$\frac{4}{27}$(用分数表示);若反应开始时,将1molN2和3molH2通入到该容器,再达新平衡时的平衡常数为K2,则K2=K1(填“>”、“<”或“=”)
(2)平衡后,若要提高H2的转化率,可以采取的措施有C.
A.加了催化剂B.充入一定量的Ne
C.降低反应体系的温度D.再充入2mol的Ne和6mol的H2
(3)其化学平衡常数K与温度T的关系如表所示:
| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1>K2(填“>”、“<”或“=”).
②400℃时,反应2NH3(g)?N2(g)+3H2(g)的化学平衡常数为2,2L的容器中,当测得NH3、N2和H2物质的量分别为6mol、4mol和2mol时,则该反应的v(N2)减>v(N2)增(填“>”、“<”或“=”).
(4)根据化学反应速率和化学平衡理论,联合合成氨的生产实际,你认为下列说法不正确的是C
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.勒夏特列原理可指导怎样使用有限原料多出产品
C.催化剂的使用是提高产品产率的有效方法
D.正确利用化学反应速率和化学反应限度理论都可以提高化工生产的综合经济效益.
9.某工厂使用石油热裂解的副产物CH4来制取H2,其生产流程如图1所示:
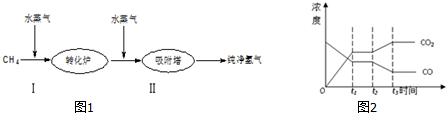
(1)第II步反应为CO(g)+H2O(g)?H2(g)+CO2(g)△H<0,其平衡常数随温度的变化如下:
在830℃下,若开始时向恒容密闭容器中充入CO与H2O均为1mo1,则达到平衡后CO的转化率为50%.
(2)第II步反应CO(g)+H2O(g)?H2(g)+CO2(g),在830℃,向恒容反应器中加入下列物质发生上述反应,其中反应开始时,向正反应方向进行的有B(填实验编号).
(3)在一个不传热的恒容容器中,判断第II步反应达平衡的标志是③④(填序号).
①体系的压强不再变化 ②混合气体的平均相对分子质量不再变化
③体系中各物质的浓度不再改变 ④体系的温度不再变化
⑤混合气体的密度不再变化
(4)图2表示此流程的第II步反应在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况.则图中t2时刻发生改变的条件是降低温度或增加水蒸汽的量或减少氢气的量(只写2种).
(5)若400℃时,第Ⅱ步反应生成l molH2放出的热量为 33.2kJ,第Ⅰ步反应的热化学方程式为 CH4(g)+H2O(g)═CO(g)+3H2(g)△H=-103.3kJ•mol-1.
则400℃时,CH4和水蒸气反应生成CO2和H2的热化学方程式为CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=-136.5kJ•mol-1.

(1)第II步反应为CO(g)+H2O(g)?H2(g)+CO2(g)△H<0,其平衡常数随温度的变化如下:
| 温度T/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(2)第II步反应CO(g)+H2O(g)?H2(g)+CO2(g),在830℃,向恒容反应器中加入下列物质发生上述反应,其中反应开始时,向正反应方向进行的有B(填实验编号).
| 实验编号 | n(CO)/mol | n(H2O)/mol | n(H2)/mol | n(CO2)/mol |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
①体系的压强不再变化 ②混合气体的平均相对分子质量不再变化
③体系中各物质的浓度不再改变 ④体系的温度不再变化
⑤混合气体的密度不再变化
(4)图2表示此流程的第II步反应在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况.则图中t2时刻发生改变的条件是降低温度或增加水蒸汽的量或减少氢气的量(只写2种).
(5)若400℃时,第Ⅱ步反应生成l molH2放出的热量为 33.2kJ,第Ⅰ步反应的热化学方程式为 CH4(g)+H2O(g)═CO(g)+3H2(g)△H=-103.3kJ•mol-1.
则400℃时,CH4和水蒸气反应生成CO2和H2的热化学方程式为CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=-136.5kJ•mol-1.
14.下列说法正确的是( )
| A. | 可以用聚氯乙烯制的薄膜来包装药品和食品 | |
| B. | 酒精杀菌消毒利用的是使蛋白质盐析的原理 | |
| C. | 碘是人体必需的微量元素之一,有“智力元素”之称 | |
| D. | 医疗垃圾中含有多种致病微生物,因此一般采用卫生填埋的方法来处理 |
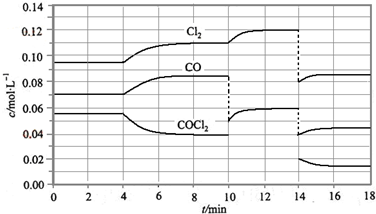
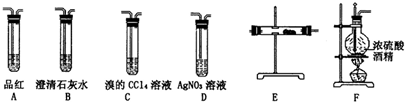 某研究小性学习小组的同学欲用如图所示的装置完成下列实验,验证制得的乙烯气体中含有SO2、CO2、水蒸气;确定乙烯与单质溴能否反应及反应类型.
某研究小性学习小组的同学欲用如图所示的装置完成下列实验,验证制得的乙烯气体中含有SO2、CO2、水蒸气;确定乙烯与单质溴能否反应及反应类型.